Glicina
composto químico From Wikipedia, the free encyclopedia
Remove ads
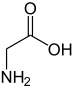
A glicina[4] (abreviadamente Gly ou G) é un α-aminoácido coa fórmula química NH2CH2COOH. A súa cadea lateral está formada só por un átomo de H, o que fai da glicina o aminoácido coa cadea lateral máis simple e o máis pequeno dos 20 aminoácidos proteicos. Os seus codóns son GGU, GGC, GGA e GGG.
- Non confundir coa planta chamada glicinia (xénero 'Wisteria') ou co xénero de plantas 'Glycine' (ao que pertence a soia).

A glicina é un sólido cristalino incoloro e doce. Forma parte das proteínas, pero tamén funciona como neurotransmisor. É único entre os aminoácidos en non ter un carbono asimétrico ou centro quiral (porque o seu carbono alfa está unido a dous substituíntes iguais, dous hidróxenos), polo que é o único aminoácido proteico que non ten isómeros D e L. Aínda que a súa cadea lateral formada por un só hidróxeno é hidrófoba, esta é tan pequena, que os grupos carboxilo e amino ionizados da molécula teñen grande influencia no conxunto, polo que pode existir establemente en medios hidrófilos ou hidrófobos.
Outro nome da glicina é glicocola[5], xa en desuso.
Remove ads
Produción e propiedades
A glicina foi descuberta en 1820, por Henri Braconnot fervendo xelatina con ácido sulfúrico.[6]
A glicina elabórase industrialmente tratando ácido cloroacético con amoníaco:[7]
- ClCH2COOH + 2 NH3 → H2NCH2COOH + NH4Cl
Prodúcense desta maneira uns 15 millóns de kg anuais.[8]
Nos Estados Unidos e o Xapón prodúcese por medio da reacción de Strecker.[9] Segundo o proceso de fabricación que se utilice pode obterse un produto final con algúns residuos de cloruro pero ningún de sulfato ou o contrario.
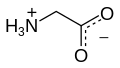
Os seus valores de pK son 2,35 e 9,78, polo que por encima do pH 9,78, a maioría da glicina está en forma de amina aniónica co grupo carboxilo ionizado, H2NCH2CO2-. Por debaixo de pH 2,35, predomina a forma de carboxilo catiónico co grupo amino ionizado H3N+CH2CO2H. O seu punto isoeléctrico (pI) é 6,06.
A glicina en solución está en forma zwitteriónica. Nesta forma, as cargas parciais nos diferentes átomos determínanse usando o método de carga de Gasteiger, e son as seguintes: N (+0.2358), H (unido ao N) (+0.1964), C alfa (+0.001853), H (unido ao C alfa) (+0.08799), C do carbonilo (+0.085) e O do carbonilo (-0.5445).
Remove ads
Biosíntese
A glicina non é esencial na dieta humana, xa que o corpo pode biosintetizala a partir de serina, que á súa vez deriva do 3-fosfoglicerato. Na maioría dos organismos, o encima serina hidroximetiltransferase cataliza esta transformación usando o cofactor fosfato de piridoxal:[10]
- serina + tetrahidrofolato → glicina + N5,N10-Metileno tetrahidrofolato + H2O
No fígado dos vertebrados, a síntese de glicina está catalizada pola glicina sintase. Esta conversión é doadamente reversible:[10]
- CO2 + NH4+ + N5,N10-Metileno tetrahidrofolato + NADH + H+ → Glicina + tetrahidrofolato + NAD+
A maioría das proteínas conteñen só pequenas cantidades de glicina. Unha notable excepción é o coláxeno, que contén un 35% de glicina.[10]
Remove ads
Degradación
A glicina degrádase por tres posibles vías. A vía principal nos animais implica a catálise feita pola glicina sintase (ou encima que escinde a glicina), que é o mesmo que interviña na biosíntese, porque a vía de degradación é a inversa da de síntese:[10]
- Glicina + tetrahidrofolato + NAD+ → CO2 + NH4+ + N5,N10-Metileno tetrahidrofolato + NADH + H+
Unha segunda vía de degradación consta de dous pasos. O primeiro é o inverso da biosíntese a partir de serina coa hidroximetil transferase. A serina convértese despois en piruvato pola serina deshidratase.[10] Por orixinar piruvato, que pode entrar na gliconeoxénese, a glicina considérase un aminoácido glicoxénico.
Na terceira vía posible de degradación, a glicina convértese en glioxilato pola acción da D-aminoácido oxidase. O glioxilato é despois oxidado pola lactato deshidroxenase hepática a oxalato nunha reacción dependente do NAD+.[10]
A vida media da glicina e a súa eliminación do corpo varía significativamente dependendo da dose. Nun estudo obtívose unha vida media para a glicina de entre 0,5 e 4,0 horas. [11]
Funcións fisiolóxicas
A glicina forma parte das proteínas, é precursor de diversos produtos naturais e funciona como neurotransmisor.
Papel como intermediario biosintético
Nos eucariotas superiores, o ácido delta-aminolevulínico, precursor chave das porfirinas, biosintetízase a partir da glicina e o succinil-CoA. A glicina proporciona a subunidade central C2N de todas as purinas.[10]
Papel como neurotransmisor
A glicina é un neurotransmisor inhibitorio que funciona no sistema nervioso central, especialmente na medula espiñal, tronco cerebral e retina. Cando os receptores de glicina das neuronas están activados, o cloruro entra na neurona polos receptores ionotrópicos, orixinando un potencial sináptico inhibitorio. A estricnina é un forte antagonista da glicina nos receptores de glicina ionotrópicos, e a bicuculina é outro antagonista máis feble.
A glicina requírese como co-agonista xunto co glutamato para os receptores NMDA (ambos os dous deben unirse ao receptor). A diferenza do papel inhibitorio da glicina na medula espiñal, nos receptores glutaminérxicos (NMDA) é excitatoria.
A dose media letal (LD50) da glicina é 7930 mg/kg en ratas (oral),[12] e xeralmente causa a morte por hiperexcitabilidade.
Algunhas probas indican que tomar 3000 mg de glicina antes de deitarse mellora a calidade do sono.[13]
Remove ads
Aplicacións
Á parte dos seus usos farmacéuticos (a glicina favorece a absorción gástrica de certos medicamentos) e técnicos, a glicina é tamén un aditivo alimentario na comida para mascotas e alimentación animal, e úsase na alimentación humana como aditivo edulcorante e potenciador do sabor. Ademais a glicina serve como axente tamponante en antiácidos, analxésicos, antitranspirantes, cosméticos, e produtos de baño. Por último, a glicina ou os seus derivados, úsanse na produción de produtos de goma escuma, fertilizantes, ou complexantes de metais,[14] e é un intermediario na fabricación do herbicida glifosato.

Remove ads
Presenza de glicina no espazo
A detección de glicina no medio interestelar é obxecto de debate.[15] En 2008, descubriuse unha molécula similar á glicina, o aminoacetonitrilo nunha nube de gas xigante da constelación de Saxitario polo Instituto de Radioastronomía Max Planck.[16] En 2009 confirmouse a detección de glicina nunha mostra recollida en 2004 procedente do cometa Wild 2 pola nave da NASA Stardust, o que foi o primeiro descubrimento de glicina extraterrestre. Os partidarios da teoría da panspermia utilizaron este dato para apoiar a súa idea de que "sementes" de vida poden viaxar polo espazo e chegar a outros planetas.[17]
Remove ads
Notas
Véxase tamén
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads