хемиско соединение From Wikipedia, the free encyclopedia
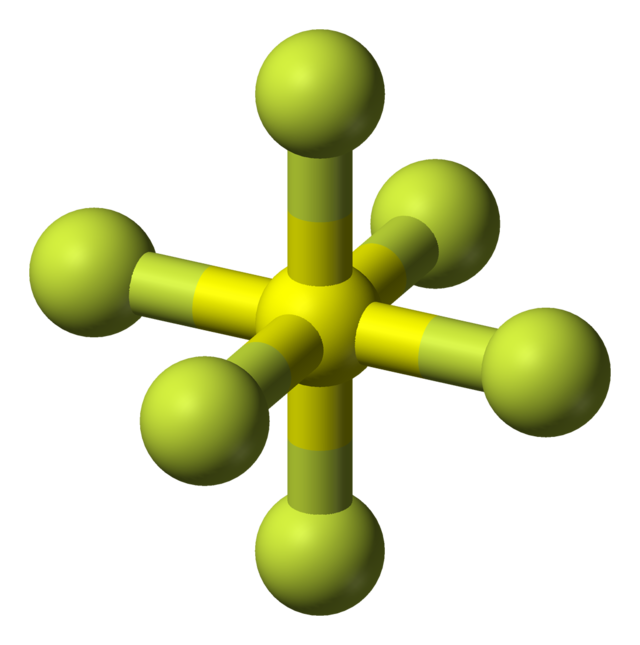
Сулфур хексафлуорид ― неорганско соединение со формулата SF6. Тоа е безбоен, без мирис, незапалив и нетоксичен гас. SF6 има октаедрална геометрија, која се состои од шест атоми на флуор прикачени на средиштен атом на сулфур. Тоа е хипервалентна молекула.
| |||
 | |||
Назив според МСЧПХ Сулфур хексафлуорид | |||
| Систематско име | Hexafluoro-λ6-sulfane[1] | ||
Други називи Елагас | |||
| Назнаки | |||
|---|---|---|---|
| 2551-62-4 | |||
| ChEBI | CHEBI:30496 | ||
| ChemSpider | 16425 | ||
| EC-број | 219-854-2 | ||
Гмелин |
2752 | ||
| 3Д-модел (Jmol) | Слика | ||
| KEGG | D05962 | ||
| MeSH | Sulfur+hexafluoride | ||
| PubChem | 17358 | ||
| RTECS-бр. | WS4900000 | ||
| |||
| UNII | WS7LR3I1D6 | ||
| ОН-бр. | 1080 | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Изглед | безбоен гас | ||
| Мирис | odorless[2] | ||
| Густина | 6.17 g/L | ||
| Точка на топење | |||
| Точка на вриење | |||
| Критична точка (T, P) | 45,51 ± 0,1 °C, 3,749 ± 0,01 MPa[3] | ||
| 0.003% (25 °C)[2] | |||
| Растворливост | малку растворлив во вода, многу растворлив во етанол, хексан, бензен | ||
| Парен притисок | 2.9 MPa (at 21.1 °C) | ||
Магнетна чувствителност (χ) |
−0 cm3/mol | ||
| Топлинска спроводливост |
| ||
| Вискозност | 15.23 μPa·s[5] | ||
| Структура | |||
| Кристална структура | Орторомпски, oP28 | ||
Просторна група |
Oh | ||
Координациска геометрија |
Орторомпски шестаголен | ||
| Геометрија на молекулата | Октахедрален | ||
| Диполен момент | 0 D | ||
| Термохемија | |||
| Ст. енталпија на образување ΔfH |
−1209 kJ·mol−1[6] | ||
| Стандардна моларна ентропија S |
292 J·mol−1·K−1[6] | ||
| Специфичен топлински капацитет, C | 0.097 kJ/(mol·K) (постојан притисок) | ||
| Pharmacology | |||
| ATC код | V08DA05 | ||
| Податоци за дозволи |
| ||
| Опасност | |||
| GHS-ознаки:[7] | |||
Пиктограми |
 | ||
Сигнални зборови |
Внимание | ||
Изјави за опасност |
H280 | ||
Изјави за претпазливост |
P403 | ||
| NFPA 704 | |||
| NIOSH (здравствени граници во САД): | |||
PEL (дозволива) |
TWA 1000 ppm (6000 mg/m3)[2] | ||
REL (препорачана) |
TWA 1000 ppm (6000 mg/m3)[2] | ||
IDLH (непосредна опасност) |
N.D.[2] | ||
| Безбедносен лист | External MSDS | ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||
Вообичаено за неполарен гас, SF6 е слабо растворлив во вода, но доста растворлив во неполарни органски растворувачи. Има густина од 6,12 г/Л при услови на морското ниво, значително повисока од густината на воздухот (1,225 г/Л). Воглавно е пренесуван како течен компримиран гас.
SF6 е 23.500 пати помоќен од јаглерод диоксидот како greenhouse gas но постои во релативно мали концентрации во атмосферата. Неговата концентрација во земјината тропосфера достигнала 10.63 делови од трилион во 2021 година, кревајќи на 0.39 делови од трилион/годишно.[8] Зголемувањето во текот на претходните 40 години било поттикнато во голем дел од проширувањето на електроенергетскиот сектор, вклучително и избегани емисии на гасот SF6 содржан во неговите средни и високо волтни трафостаници. Употребата во производството на магнезиум, алуминиум и електроника, исто така, го забрза атмосферскиот раст.[9]
Сулфур хексафлуорид на Земјата постои првенствено како вештачки индустриски гас, но исто така е откриено дека се јавува природно.[10]
SF6 може да биде подготвен од елементите преку изложување на S8 кон F2. Исто така, ова бил методот користен од страна на пронаоѓачите Анри Моасан и Пол Лебо во 1901 година. Некои други сулфур флуориди се заедно створени, но овие се извадени со загревањето на смесата за да диспропорционира било кој S2F10 (кој е многу токсичен) и потоа чистејќи го производот со NaOH за да биде уништен останатиот SF4.
Алтернативно, со користење на бром, сулфур хексафлуорид може да се синтетизира од SF4 и CoF3 на пониски температури (на пр. 100 °C), како што следува:[11]
Практично нема реакција хемија за SF6. Главниот придонес за инертноста на SF6 е стеричната пречка на сулфурниот атом, додека неговите потешки соседни атоми од групата 16, како што е SeF<sub id="mwbQ">6</sub> се пореактивни од SF6 како резултат на помала стерична пречка.[12] Не реагира со стопениот натриум под неговата точка на вриење,[13] туку реагира егзотермно со литиумот.
Електроенергетската индустрија користела околу 80% од сулфур хексафлуорид произведен во 2000 година, главно како гасовита диелектрична средина.[14] Други главни употреби заклучно со 2015 година вклучувале силиконски елаборат за производство на полупроводници и инертен гас за лиење на магнезиум.[15]
Сулфур хексафлуорид бил трагачкиот гас што бил користен во првата калибрација на моделот за раширување на воздухот на патиштата; оваа истражувачка програма била спонзорирана од Агенцијата за заштита на животната средина на Соединетите Држави и спроведена во Санивејл, Калифорнија на Автопатот 101.[16] Гасовит SF6 е користен како гас за следење во краткорочни опити за ефикасност на вентилација во згради и затворени простории и за одредување на стапките на инфилтрација. Два главни фактори ја препорачуваат неговата употреба: неговата концентрација може да се мери со задоволителна точност при многу ниски концентрации, а атмосферата на Земјата има занемарлива концентрација на SF6.
Сулфур хексафлуоридот бил искористен како нетоксичен тест гас во опит на метро станицата „Сент Џонс Вуд“ во Лондон, Обединетото Кралство на 25 март 2007 година.[17] Гасот бил испуштен низ станицата и бил следен додека се движел наоколу. Целта на опитот, кој претходно во март бил најавен од државниот секретар за транспорт, Даглас Александар, била да се истражи како отровниот гас може да се прошири низ станиците и зградите на лондонското метро за време на терористички напад.
Сулфур хексафлуоридот, исто така, рутински е користен како гас за следење во лабораториското тестирање за задржување на аспираторот. Гасот е користен во последната фаза од квалификацијата на аспираторот ASHRAE 110. Во внатрешноста на аспираторот се создава столб од гас и се врши низа на тестови додека анализатор на гас е поставен надвор од примероците на аспираторот за SF6 за да ги потврди својствата на задржување на аспираторот.
Успешно се користи како трагач во океанографијата за проучување на дијапиктно мешање и размена на гасови од воздух-море.[18]
Сулфур хексафлуорид е нетоксичен гас, но со поместување на кислородот во белите дробови, тој исто така носи ризик од асфиксија ако се вдишува премногу.[30] Бидејќи е погуст од воздухот, значителна количина на гас, кога ќе се ослободи, ќе се насели во ниските области и ќе претставува значителен ризик од асфиксија ако се влезе во областа. Тоа е особено важно за неговата употреба како изолатор во електрична опрема бидејќи работниците може да бидат во ровови или јами под опремата што содржи SF6.[31] Како и кај сите гасови, густината на SF6 влијае на фреквенциите на резонанца на гласниот тракт, со што драстично се менуваат гласните квалитети на звукот или темброт на оние кои го вдишуваат. Тоа не влијае на вибрациите на гласните набори. Густината на сулфур хексафлуорид е релативно висока на собна температура и притисок поради големата моларна маса на гасот. За разлика од хелиумот, кој има моларна маса од околу 4 g/mol и го крева гласот, SF6 има моларна маса од околу 146 g/mol, а брзината на звукот низ гасот е околу 134 m/s на собна температура, спуштајќи го гласот. За споредба, моларната маса на воздухот, која е околу 80% азот и 20% кислород, е приближно 30 g/mol што доведува до брзина на звукот од 343 m/s.[32]
Сулфур хексафлуорид има анестетичка моќ малку пониска од азот оксид;[33] тој е класифициран како слаб анестетик.[34]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.