From Wikipedia, the free encyclopedia
ABC-транспортери (англиски: ATP-binding cassette transporters — ATP-врзувачки касетни транспортери) — членови на натсемејство на транспортни системи, која е една од најголемите и веројатно едно од најстарите семејства со претставници во сите колена на живиот свет, од прокариоти па сѐ до човекот.[1][2]


ABC-транспортерите често се изградени од повеќе подединици, од кои една или две се трансмембрански белковини и една или две се мембрански асоцирани ААА-ATPази. ATPазните подединици ја користат енергијата од врзувањето и хидролизата на ATP за да ја покренат транслокацијата на различни супстрати низ мембраната, без разлика дали е за внесување или изнесување на супстратот.
Повеќето, но не сите, системи за внесување имаат и екстрацитоплазматски рецептор кој го врзува супстратот. Некои хомологни ATPази учествуваат во процеси кои не се поврзани со транспорт, како што се на пример транслацијата на РНК и поправката на ДНК.[3][4] ABC-транспортерите се класифицираат во ABC-натсемејството на белковини, врз основа на низата и организацијата на нивните ATP-врзувачки касетни (ABC) домени, иако нивните интегрални мембрански домени еволуирале независно едни од други неколкупати во еволуционата историја на животот, што ги прави да припаѓаат на различни белковински семејства. Интегралните мембрански белковини на ABC-извозниците (изнесувачите) еволуирале независно едни од други најмалку трипати во историјата на животот.[5] Врз основа на нивните тридимензионални структури со висока резолуција, веројатно е дека интегралните мембрански белковини на ABC-увозниците (внесувачите) еволуирале независно едни од други најмалку трипати.[6] ABC-увозниците во клетката внесуваат разни молекули, како што се: хранливи материи, биосинтетски претходници, витамини, метални јони; додека ABC-извозниците изнесуваат од клетката стероли, липиди, ксенобиотици и голем број на првични и вторични метаболити. Високото ниво на експресија на гените кои кодираат некои од овие извозници и кај прокариотските и кај еукариотските организми (вклучувајќи го и човекот) резултира со развој на отпорност кон многу лекови, како што се антибиотици и антиканцерогени лекови.
Досега се одликувани стотици ABC-транспортери и кај прокариотите и кај еукариотите.[7] Бидејќи ABC-гените, кои кодираат за овие белковини, се од клучно значење за многу клеточни процеси, мутациите кои се јавуваат кај нив може да резултираат со тешки генетски заболувања.[8] Кај човекот има 48 гени кои кодираат за ABC-транспортери. Мутациски промени на повеќето од нив може да резултираат со тешки заболувања како што се: цистична фиброза, адренолеукодистрофија, Штаргардтова болест, тумори отпорни на антиканцерогени лекови, сидеробластна анемија, атаксија, итн.[7] ABC-транспортерите се исто така одговорни за отпорност кон повеќе лекови; на пример, кога се јавува многу висока експресија на ABC-гените во туморските клетки, тие стануваат отпорни на многу антиканцерогени лекови.[9]
ABC-транспортерите ја користат врзивната енергија и хидролиза на ATP за транспорт на различни супстрати низ клеточните мембрани. Тие можат да се поделат во три главни функционални категории. Кај прокариотите, увозниците посредуваат во внесувањето на хранливи материи (нутриенси) во клетката. Супстратите кои се внесуваат се: јони, аминокиселини, шеќери, пептиди и други главно хидрофилни молекули. Мембранскиот регион на ABC-транспортерот го штити хидрофилниот супстрат од мембранските липиди и на тој начин му овозможува непопречен пат низ мембраната. Еукариотските организми не поседуваат увозници, но тие поседуваат извозници, кои се присутни и кај прокариотите, а функционираат како пумпи кои исфрлаат токсични материи и лекови од клетката. Кај Грам-негативните бактерии, извозниците служат и за транспорт на липиди и некои полисахариди од цитоплазмата во периплазмата. Третата подгрупа на ABC белковини не играат улога на транспортери туку се вклучени во процесите на транслација и поправка на ДНК.[3]
Бактериските ABC-транспортери се неопходни за одржување на вијабилноста на клетката, а кај патогените видови и за нивна вирулентност и патогеност.[3] На пример, ABC-системите за внесување на железни јони кај бактериите се битни ефектори на вирулентност.[10] Патогените бактерии користат сидерофори, како што е ентеробактинот, за да го врзат железото кое е во комплекс со високоафинитетни железо-врзувачки белковини или еритроцити. Сидерофорите се органски молекули кои го хелираат железото со многу висок афинитет. Нив ги излачува бактериската клетка во околината богата со железо, по што ги реапсорбира во облик на сидерофор-железен комплекс преку посебни ABC-транспортни системи. Кај бактеријата Agrobacterium tumefaciens, генот chvE-gguAB кодира увозници за гликоза и галактоза, кои исто така се поврзани со вирулентноста на овој вид.[11][12] ABC-транспортерите се толку битни за опстанокот на клетката што тие функционираат како белковински системи кои се спротивставуваат на разни видови на непожелни промени и дисбаланси кои може да се случат во клетката. На пример, при смртоносно зголемување на осмотскиот притисок во клетката, се активираат осмосензорни ABC-транспортери кои посредуваат во внесувањето на растворливи супстанци.[13] Покрај тоа што учествуваат во транспортот на материи, некои бактериски ABC-белковини можат да бидат вклучени и во регулација на неколку физиолошки процеси.[3]
Бактериските експортни системи изнесуваат од клетката разни супстрати: градбени компоненти на клеточниот ѕид (липополисахариди, теихонски киселини), белковини инволвирани во бактериската патогенеза (пр. хемолиза, хем-врзувачка белковина и алкална протеаза), хидролитички ензими, белковини на S-слојот, токсини, антибиотици, бактериоцини, сидерофори, итн.[14] Тие, исто така, играат значајни улоги и во некои биосинтетски патишта, вклучувајќи ја биосинтезата на вонклеточните полисахариди[15] и биогенезата на цитохромите.[16]
Иако повеќето еукариотски ABC-транспортери се извозници, некои не се директно вклучени во транспортот на супстратите. Кај трансмембранскиот регулатор на цистична фиброза (CFTR, од англ. cystic fibrosis transmembrane regulator), хидролизата на ATP е поврзана со отворањето и затворањето на јонските канали кои ги носи самата ABC-белковина.[4]
ABC-транспортерите кај човекот се поврзани со повеќе болести кои настануваат како резултат на полиморфизми во ABC-гените, а ретко поради целосното губење на функцијата на една ABC-белковина.[17] Вакви заболувања вклучуваат Менделови болести и комплексни генетски нарушувања, како што се: цистична фиброза, адренолеукодистрофија, Штаргардтова болест, Тангиерска болест, имунолошка дефициентност, прогресивно семејна интрахепатична холестаза, синдром на Дабин-Џонсон, Pseudoxanthoma elasticum, перзистентна хиперинсулинемична хипогликемија во детството поради фокална аденоматозна хиперплазија, X-поврзана сидеробластна анемија, макуларна дегенерација поврзана со возраст, семејна хипоапопротеинемија, Retinitis pigmentosum, корнеална дистрофија и други.[4] ABCB (MDR/TAP)-семејството кај човекот е одговорно за отпорност кон повеќе лекови (MDR, од англ. multiple drug resistance). ABCB1 или MDR1 P-гликобелковината е вклучена и во други биолошки процеси, главно за транспорт на липидни молекули. Тој посредува во секреција на стероидниот хормон алдостерон, кого го излачуваат адреналните жлезди, а се покажало дека неговата инхибиција ја спречува миграцијата на дендритичните имуни клетки,[18] веројатно како резултат на транспортот на тромбоцит-активирачкиот фактор. Познато е дека ABCB1 посредува во транспортот на кортизол и дексаметазон, но не и на прогестерон во ABCB1-трансфектираните клетки. MDR1 исто така може да транспортира холестерол, кратковерижни и долговерижни аналози на фосфатидилхолин (PC), фосфатидилетаноламин (PE), фосфатидилсерин (PS), сфингомиелин (SN) и гликозилцерамид (GlcCer). Мултиспецифичниот транспорт на разновидни ендогени липиди преку MDR1-транспортерот може да влијае на трансдвослојната дистрибуција на липидите, главно на липидните молекули кои се повеќе застапени во внатрешниот слој од мембраната, како што се PS и PE.[17]
Во поново време, покажано е дека ABC-транспортерите се застапени во плацентата, каде веројатно играат заштитна улога, штитејќи го фетусот во развој од штетното дејство на ксенобиотици.[19]


Заедничката одлика на сите ABC-транспортери е што тие се состојат од два посебни домена, трансмембрански домен (TMD) и нуклеотид-врзувачки домен (NBD).[20] TMD е изграден од алфа-завојницаи кои се вградени во фосфолипидниот двослој на мембраната. Овој домен препознава мноштво на супстрати и подлежи на конформациски промени преку кои е овозможен транспорт на овие супстрати низ мембраната. Аминокиселинската низа и архитектурата на TMD е променлива, што ја одразува хемиската разновидност на супстратите кои биваат транссместени. NBD, или ATP-врзувачкиот касетен (ABC) домен, се наоѓа во цитоплазмата и, за разлика од TMD, има високо сочувана аминокиселинска низа. NBD го содржи активното место за врзување на молекула на ATP.[21] Кај најголемиот број на извозници, N-терминалниот трансмембрански домен и C-терминалниот ABC домен се споени во еден полипептиден ланец, кој е организиран во редоследот TMD-NBD-TMD-NBD. увозниците, пак, имаат обратна организација, NBD-TMD-NBD-TMD, при што ABC доменот е N-терминален, а TMD е C-терминален.[3][4]
Структурната архитектура на ABC-транспортерите се состои од минимум два TM домена и два NB домена. Можат да бидат искомбинирани четири поединечни полипептидни ланци (два TMD и два NBD) за формирање на целосен транспортер, како кај BtuCD импортерот на E. coli кој учествува во внесувањето на витамин Б12.[22][23] Поголемиот број на извозници, како што е Sav1866[24] кај S. aureus, кој изнесува повеќе лекови, се изградени од хомодимери, кој се состои од два полутранспортери, односно мономери, составени од еден TMD споен со еден NBD. За да белковината биде функционална, најчесто е неопходно транспортерот да биде целосен. Одделни ABC-транспортери поседуваат додатни елементи кои придонесуваат во регулаторната функција на оваа класа на белковини. Така, увозниците поседуваат врзувачка белковина (BP, од англ. binding protein) со висок афинитет, кој специфично се врзува за супстратот во периплазмата, по што го испорачува на соодветниот ABC-транспортер. Извозниците, пак, немаат врзувачка белковина, но поседуваат внатреклеточен домен (ICD) кој се надоврзува на трансмембранските завојници и на ABC доменот. Се смета дека ICD е одговорен за комуникација помеѓу TMD и NBD.[21]
Мнозинството на ABC-транспортери имаат трансмембрански домен кој се состои од вкупно 12 алфа-завојницаа, со шест алфа-завојницаа по мономер. Бидејќи TM домените се структурно разновидни, поединечните транспортери имаат различен број на алфа-завојници (помеѓу 6 и 11). TM домените се категоризирани во три посебни сета на набори (англ. folds): тип I ABC импортер, тип II ABC импортер и ABC извозник. Класификацијата на наборите на увозниците е заснована на детална карактеризација на нивните низи.[21] Тип I ABC импортер наборот првично бил забележан во ModB TM подединицата на транспортерот на молибдатни јони.[25] Овој дијагностички набор исто така е присутен и во MAIF и MAIG TM подединиците на MAIFGK2[26] и MetI транспортерот.[27] Кај MetI транспортерот, минимален сет од пет трансмембрански алфа-завојници го сочинуваат овој мотив, додека кај ModB и MAIG присутен е еден дополнителен алфа-завојница. Општата организација на овој мотив е „горе-долу“ топологија на ТМ2-5 завојницата која ја обиколува транслокационата стаза и ТМ1 завојницата обвиткана околу надворешната мембранска површина и е во контакт со другите ТМ завојници. Тип II ABC увозничкиот мотив е забележан во дваесет ТМ завојните домени на BtuCD[22] и во Hi1471,[28] хомологниот транспортер од Hemophilus influenzae. Кај BtuCD, пакувањето на алфа-завојниците е комплексно. Често ТМ2 завојницата зазема позиција низ центарот на подединицата, каде е обиколен со други завојници. ТМ5 и ТМ10 завојниците се сместени на ТМD интерфејсот. Кај ABC извозниците, регионот кој ја премостува мембраната е организиран во две „крила“ кои се состојат од завојниците ТМ1 и ТМ2 од едната подединица и ТМ3-6 од другата подединица, во аранжман на доменска размена. Често се случува завојниците ТМ1-3 да се сродни со завојниците ТМ4-6 во смисла на приближната двојна ротација околу оската во рамнината на мембраната.[21]

ABC доменот се состои од два поддомена, централен каталитички домен, кој наликува на RecA-сличните ATPазни мотори, и помал, структурно разновиден, алфа-завоен поддомен, кој единствено се среќава кај ABC-транспортерите. Поголемиот домен типично се состои од две бета плочи и шест алфа-завојницаа, каде е сместен каталитичкиот Вокеров А мотив (GXXGXGKS/T, каде X е која било аминокиселина), кој уште се нарекува и P-петелка, и Вокеровиот B мотив (ΦΦΦΦD, каде Φ е хидрофобна аминокиселина). Помалиот, завоен домен се состои од три или четири завојници и ABC-специфичниот мотив, кој е познат и како LSGGQ мотив или С мотив. ABC доменот исто така има и глутамински остаток во флексибилната петелка позната како Q петелка, капаче или γ-фосфатен прекинувач, кој ги поврзува TM и ABC домените. Се смета дека Q петелката е вклучена во интеракцијата на NBD и TMD, особено во поврзаноста (спрегата) меѓу хидролизата на ATP и конформационите промени на TMD во текот на транслокацијата на супстратот. Н мотивот, познат и како прекинувачки регион, содржи високо сочуван хистидински остаток, кој е важен во интеракцијата на ABC доменот со ATP. Името ATP-врзувачка касета е изведено од специфичниот аранжман на наборите или мотивите на оваа класа на белковини по формирањето на ATP сендвич и хидролизата на ATP.[3][14][21]
Врзувањето на ATP е неопходно за формирање на димер на двата ABC домени од транспортерот.[29] Интерфејсот помеѓу ABC домените е најекстензивен кога тие имаат врзано ATP молекули, а кога немаат врзано ATP конформацијата на белковината е таква што постои максимална раздвоеност на ABC-домените.[21] Структурите на изолирани NB домени, во состојба кога имаат врзано ATP, се познати кај следните увозници: HisP,[30] GlcV,[31] MJ1267,[32] E. coli MalK (E.c. MalK),[33] T. litoralis MalK (TLMalK),[34] и кај следните извозници: TAP,[35] HlyB,[36] MJ0796,[37][38] Sav1866,[24] и MsbA.[39] Двете молекули на ATP се позиционираат во интерфејсот на димерите, помеѓу Вокеровиот А мотив на едната подединица и LSGGQ мотивот на другата подединица.[21] Оваа конфигурација првпат била воочена кај Rad50[40] и во структурите на MJ0796, NBD подединицата на LolD транспортерот на Methanococcus jannaschii[38] и E.c. MalK малтозниот транспортер.[33] Структурите се, исто така, доследни со резултатите добиени од биохемиски испитувања, кои покажале дека ATP е во близок контакт со аминокиселинските остатоци на P-петелката и LSGGQ мотивот во текот на каталитичкиот процес.[41]
Врзувањето на ATP е неопходно за да се осигура електростатичен и структурен интегритет на активното место и да се поттикне формирањето на активниот NBD димер.[42] Врзувањето на ATP се стабилизира со помош на следните заемодејства: (1) стекинг интеракција (англ. stacking interaction) помеѓу прстенот на сочувана ароматична аминокиселина, која претходи на Вокеровиот А мотив, и аденинскиот прстен на ATP молекулата,[43][44] (2) водородни врски помеѓу сочуваниот лизински остаток од Вокеровиот А мотив и кислородните атоми на бета- и гама-фосфатот од ATP молекулата и координација на овие фосфати и одредени аминокиселински остатоци од Вокеровиот А мотив со Mg2+ јон,[31][35] и (3) координација на гама-фосфатот со страничниот ланец на серинот и амидните групи од делот на полипептидната верига каде се наоѓаат глицинските остатоци во LSGGQ мотивот.[45] Дополнително, сочуваниот хистидин во Н-петелката ја поттикнува димеризацијата на домените по врзувањето на ATP. Овој хистидински остаток стапува во контакт со аминокиселински остатоци во Вокеровиот А мотив и D петелката од другата страна на димерниот интерфејс.[33][38][40][46]
Правилното врзување на фосфатните остатоци и позиционирањето на гама-фосфатот кон молекулата на вода која го напаѓа е неопходно за ензиматската хидролиза на ATP.[21] Во активното место на врзување на нуклеотидот, кислородните атоми на бета- и гама-фосфатите на ATP молекулата биваат стабилизирани од аминокиселинските остатоци на Вокеровиот А мотив[47][48] и преку координација со Mg2+ јонот.[21] Mg2+ јонот, исто така, се координира со терминалниот аспартатен остаток од Вокеровиот В мотив преку молекулата на вода која напаѓа.[31][32][37] Генерална база, која може да биде глутаматниот остаток веднаш до Вокеровиот B мотив,[29][38][44] глутаминот во Q-петелката,[28][34][38] или хистидинот во прекинувачкиот регион кој формира водородна врска со гама-фосфатот од ATP молекулата, ја катализира брзината на хидролиза на ATP со промовирање на напаѓачката молекула на вода.[33][34][38][46] Точниот молекуларен механизам на хидролизата на ATP сè уште не е целосно утврден.[3]
ABC-транспортерите се активни транспортери т.е. потребна е енергија во форма на ATP за транслокација на супстратот преку клеточната мембрана. Овие белковини ја искористуваат врзивната енергија и/или хидролиза на ATP за поттикнување на конформациони промени во трансмембранскиот домен (TMD) кои се одговорни за транспортот на супстратните молекули.[49] ABC увозниците и извозниците имаат сличен механизам на транспорт на супстрати што произлегува од сличностите во нивните структури. Механизмот кој ги опишува конформационите промени на транспортерот одговорни за врзување на супстратот се нарекува модел на наизменичен пристап. Во овој модел, местото за врзување на супстратот се менува меѓу конформација која е насочена кон надворешноста и конформација која е насочена кон внатрешноста. Релативните афинитети за врзување на супстратот на двете конформации ја одредуваат насоката на транспортот. Кај увозниците, бидејќи транслокацијата е насочена од периплазмата кон цитоплазмата, тогаш конформацијата која е насочена кон надворешноста ќе има повисок афинитет за врзување на супстратот. Спротивно на ова, кај извозниците конформацијата која е насочена кон внатрешноста ќе има повисок афинитет за врзување на супстратот.[21] Моделот кој ги опишува конформационите промени во нуклеотид-врзувачкиот домен (NBD), како резултат на врзувањето и хидролизата на ATP, се нарекува ATP-прекинувачки модел (англ. ATP-switch model). Овој модел предвидува две главни конформациони промени на NBD: создавање на затворен димер по врзувањето на две ATP молекули и дисоцијација во отворен димер по хидролиза на ATP и ослободување на ADP и неоргански фосфат (Pi). Премините помеѓу отворена и затворена конформација на димерот предизвикуваат конформациски промени во TMD, што резултира со транслокација на супстратот.[50]
Општиот механизам за транспортниот циклус на ABC-транспортерите сè уште не е целосно разјаснет, сепак акумулирани се прилично голем број на структурни и биохемиски податоци за поддршка на моделот во кој врзувањето и хидролизата на ATP е спрегнато со конформациските промени одговорни за транслокација на супстратот. Во состојба на мирување на сите ABC-транспортери, NB домените се наоѓаат во отворена димерна конфигурација, со низок афинитет за ATP. Оваа отворена конформација поседува комора која е достапна на внатрешноста на транспортерот. Циклусот на транспортот започнува со врзување на супстратот за одредено место на TMD кое има висок афинитет кон него, што предизвикува конформациони промени во NBD кои го зголемуваат афинитетот за врзување на ATP. Потоа, две молекули на ATP се врзуваат кооперативно за NBD, за да ја формираат конфигурацијата на затворен димер. Затворениот NBD димер индуцира конформациони промени во TM домените, кои предизвикуваат отворање на TMD и формирање на комора со отвор кој е спротивен на оној од почетната состојба. Афинитетот на TMD кон супстратот се намалува, па тој го отпушта во околината. По ова следи хидролиза на ATP со последователно ослободување на Pi, а потоа и на ADP, што дејствува да го врати транспортерот во неговата првобитна (основна) конфигурација. Иако е предложен општ механизам, сепак, сè уште се дебатира за точниот редослед на врзување на супстратот, врзувањето и хидролизата на ATP, конформациските промени, како и заемодејствата помеѓу домените.[3][14][17][21][39][42][49][50][51][52][53]
Неколку истражувачки групи кои ги проучуваат ABC-транспортерите имаат различни теории во поглед на механизмот на дејството на транспортерите. Сè до неодамна генерално било прифатено дека хидролизата на ATP го обезбедува главниот енергетски инпут или погон за транспорт на супстратот и дека NB домените делуваат наизменично, како и дека е можно да учествуваат во различни чекори од транспортниот циклус.[54] Меѓутоа, најновите структурни и биохемиски податоци укажуваат на тоа дека врзувањето на ATP, а не неговата хидролиза, е главниот погон за транспортот на супстратот. Бидејќи врзувањето на ATP ја иницира димеризацијата на NBD, можно е формирањето на димерот да претставува главниот погон. Познато е дека некои транспортери имаат NB домени со различни способности за врзување и хидролиза на ATP, а фактот што интерфејсот на NBD димерот содржи две места за врзување на ATP сугерира дека функцијата на двата NBD во транспортниот циклус се совпаѓа.[50]
Постојат одредени докази дека врзувањето на ATP е, всушност, главниот поттикнувач на транспортниот циклус.[50] Покажано е врзувањето на ATP ги менува својствата на врзувањето на супстратот за TMD. Афинитетот на ABC-транспортерот за неговиот супстрат тешко се мери директно, а индиректните мерења, на пример со стимулација на активноста на ATPазата, често ги одразуваат другите чекори од кои зависи брзината на реакцијата. Неодамна било покажано, со директни мерења на врзување на винбластин за пермеазниот гликобелковина (P-гликобелковина) во присуство на нехидролизирачки аналози на ATP (пр. 5’-аденилил-β-γ-имидодифосфат, AMP-PMP), дека врзувањето на ATP, во отсуство на хидролиза, е доволно за да се намали афинитетот со кој TMD го врзува супстратот.[55] Исто така, врзувањето на ATP индуцира значителни конформациони промени во двата TM домена. Спектроскопските истражувања, испитувањата на протеазната пристапност и истражувањата со вкрстено врзување покажале дека врзувањето на ATP за NB домените индуцира конформациони промени кај MRP1 (англ. multidrug resistance-associated protein-1),[56] HisPMQ,[57] LmrA[58] и Pgp.[59] Дводимензионалните кристални структури на AMP-PMP врзан за Pgp покажале дека во текот на транспортниот циклус најголемите конформациони промени се случуваат по врзувањето на ATP, а последователната хидролиза на ATP предизвикува поограничени промени.[60] Придонес за овие конформациони промени може да даваат вртежните движења и искривувањата на трансмембранските алфа-завојници. Други студии се имаат фокусирано на потврдување дека врзувањето на ATP го индуцира создавањето на затворениот NBD димер. Биохемиските испитувања на интактните транспортни комплекси сугерираат дека конформационите промени во NB домените се релативно мали. Во отсуство на ATP, NB домените веројатно се флексибилни, но овие движења не вклучуваат големи реориентации на NBD во однос на другите домени од транспортерот. Врзувањето на ATP индуцира ригидна ротација на двата ABC поддомени еден во однос на друг, што овозможува правилно подредување на нуклеотидите во нивните активни места и интеракција со соодветните мотиви. Постојат цврсти биохемиски докази дека врзувањето на двете ATP молекули е кооперативно, т.е. и двете молекули мора да се врзат во нивните активни места пред NB домените да можат да се димеризираат и да ја формираат затворената, каталитички активна, конформација.[50]
Повеќето ABC-транспортери кои посредуваат во внесувањето на нутриенсите и другите молекули во бактериската клетка зависат од посебни белковини за врзување на супстратот, кои го врзуваат со многу висок афинитет. Овие белковини се водорастворливи, хидрофилни белковини, кои се сместени во периплазматскиот простор кај Грам-негативните бактерии. Грам-позитивните бактерии немаат периплазматски простор, па затоа нивниот врзувача белковина најчесто е липобелковина кој е врзан за надворешната страна на клеточната мембрана. Некои Грам-позитивни бактерии имаат врзувачки белковини кои се врзани за трансмембранскиот домен на самиот ABC-транспортер.[3] Првата успешно добиена кристална структура на неоштетен ABC импортер е молибденскиот транспортер (ModBC-A) од Archaeoglobus fulgidus.[25] Одредени се и структурите на три други бактериски увозници, со атомска резолуција, и тоа: E. coli BtuCD,[22] E. coli-малтозен транспортер (MalFGK2-E),[26] и можен метал-хелатен транспортер на Haemophilus influenzae HI1470/1.[28] Структурите даваат детална слика за интеракцијата помеѓу трансмембранскиот домен и ABC-доменот. Тие, исто така, откриваат две различни конформации кај кои отворот се наоѓа на спротивни краеви. Откриено е и уште едно заедничко својство на сите увозници, а тоа е дека секој NBD се врзува за еден TMD преку краток цитоплазматски алфа-завојница на TM-доменот кој се нарекува „спрегнувачка завојница“.
BtuCD и HI1470/1 се класифицирани како големи ABC-увозници. Трансмембранската подединица на импортерот на витамин Б12, BtuCD, содржи десет трансмембрански завојници, а функционалната единица и се состои од две копии, од кои секоја има домен за врзување на нуклеотиди (NBD) и трансмембрански домен (TMD). TMD и NBD стапуваат во меѓусебна интеракција преку една цитоплазматска петелка помеѓу два TM-завојници и Q-петелката во ABC-доменот. Во отсуство на врзани нуклеотиди, постојат два ABC-домена и интерфејсот на димерот е отворен. Споредбата на структурите со врзувачка белковина (BtuCDF) и без врзувачка белковина (BtuCD) открива дека BtuCD има отвор кон периплазмата, додека кај BtuCDF-конформацијата која е насочена кон надвор е затворена и од двете страни на мембраната. Структурите на BtuCD и неговиот хомолог, HI1470/1, претставуваат две различни конформациони состојби на ABC-транспортерот. Предвидениот пат за транслокација на супстратот во BtuCD е отворен кон периплазмата, а затворен од цитоплазматската страна на мембраната, додека оној кај HI1470/1 има спротивна насока и е отворен само од цитоплазматската страна. Разликата во структурите е во свртување од 9° на едната TM-подединица во однос на другата.[3][21][52]
Структурите на ModBC-A и MalFGK2-E, кои се наоѓаат во комплекс со нивната врзувачка белковина, одговараат на мали ABC-увозници. TMD на ModBC-A и MalFGK2-E имаат само шест завојници во рамките на една подединица. Хомодимерот на ModBC-A се наоѓа во конформација во која TM-подединиците (ModB) се ориентирани во превртена V-форма, со отвор од цитоплазматската страна на мембраната. Од друга страна, ABC-подединиците (ModC) се наоѓаат во отворена конформација, без врзани нуклеотиди, во која P-петелката од едната подединица е одвоена од LSGGQ-мотивот на другата подединица. Врзувачката белковина ModA се наоѓа во затворена конформација, во која супстратот е врзан во жлебот помеѓу двата сегменти на белковинската молекула и стапува во интеракција со вонклеточните петелки на ModB, така што тој е сместен директно над затворениот влез на транспортерот. Структурата на MalFGK2-E потсетува на каталитичката транзициона состојба за хидролиза на ATP. Таа се наоѓа во затворена конформација, во која содржи две ATP-молекули позиционирани меѓу Вокеровите А и В-мотиви од едната подединица и LSGGQ мотивот од другата подединица. Малтозоврзувачката белковина (MBP или MalE) се наоѓа укотвен на периплазматската страна на TM подединиците (MalF и MalG), а на интерфејсот на овие две подединици може да се забележи една голема, затворена шуплина. Трансмембранските завојници се така поредени што формираат конформација на белковината која е затворена кон цитоплазматската страна, а отворена кон периплазматската страна. Ваквата структура сугерира дека MBP треба да се врзе за транспортерот за да ја стимулира неговата ATPазна-функција.[3][21][52]
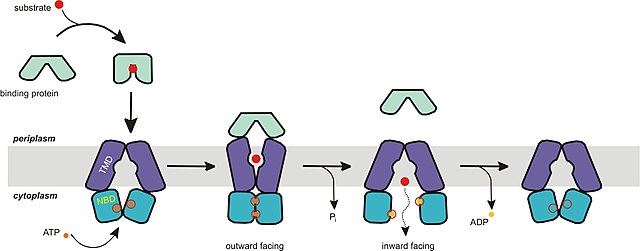
Механизамот на транспорт на ABC-увозниците го поддржува моделот на наизменичен пристап. Во состојба на мирување увозниците се насочени кон внатрешната страна, каде интерфејсот на димерот на нуклеотид-врзувачките домени (NBD) се одржува отворен од страна на трансмембранските домени (TMD) и насочен кон надворешната страна, но е затворен од спротивната, цитоплазматска, страна. По закотвувањето на затворената врзувачка белковина, кој има врзано супстрат, на периплазматската страна на TMD, доаѓа до врзување на ATP и затворање на NBD-димерот. Ова предизвикува премин на транспортерот од состојба на мирување во конформација насочена кон надворешноста, во која TMD се преориентирани за да го примат супстратот од врзувачката белковина. По хидролизата на ATP, NBD димерот се отвора и супстратот се ослободува во цитоплазмата. Отпуштањето на ADP и Pi од NBD го враќа транспортерот во состојба на мирување. Единствената противречност на овој механизам со моделот на ATP-прекинувач е што конформацијата во состојбата на мирување, каде нема врзано нуклеотид, е различна од очекуваната конформација насочена кон надворешноста. Иако ова е случајот, треба да се напомене дека NBD не се димеризира сè додека ATP и врзувачката белковина не се врзат за транспортерот.[3][14][21][50][52]
ABC-извозниците се чести во прокариотскиот свет и тие имаат блиски хомолози кај еукариотите. Тие се класифицираат според типот на супстратот кој го транспортираат. Една група на транспортери учествуваат во процесот на изнесување на белковини од клетката (пр. токсини, хидролитички ензими, белковини на S-слојот, полициклични пептидни антибиотици, бактериоцини и фактори на компетенција), а другата група учествува во процесот на изнесување на ксенобиотици (лекови). Овие ABC-извозници имаат привлечено големо внимание затоа што придонесуваат за отпорноста на клетките на дејството на антибиотици и антиканцерогени лекови, така што ги испумпуваат овие лекови од клетката.[3]
Кај Грам-негативните бактерии, ABC-извозниците посредуваат во симултаната секреција на белковинските супстрати низ внатрешната и надворешната мембрана без директен премин низ периплазмата. Овој тип на секреција се нарекува тип I секреција, а опфаќа три компоненти кои заедно функционираат: ABC-извозник, мембранска фузиона белковина (MFP) и фактор на надворешната мембрана (OMF). Пример за ваква секреција е излачувањето на хемолизин (HlyA) од E. coli, каде ABC-транспортерот на внатрешната мембрана (HlyB) формира заемодејства со фузиона белковина на внатрешната мембрана (HlyAD) и факторот на надворешната мембрана (TolC). TolC овозможува хемолизинот да биде транспортиран низ двете мембрани, без контакт со периплазмата.[14]
Отпорноста на бактериите кон лекови станува сè поголем здравствен проблем. Еден од механизмите на отпорноста на бактериите кон лекови е зголемениот ефлукс на антибиотиците од бактериската клетка. Отпорноста на лекови поради ефлукс кој е посредуван од P-гликобелковината, првично била забележана кај клетките на цицачите. Леви и неговите соработници (Levy et al.) први објавиле докази дека отпорноста на бактериите кон антибиотици може да се должи на ефлукс на лековите од бактериската клетка.[61] P-гликобелковината е најдобро проучената ефлуксна пумпа и како таква дава значаен увид во механизмот на бактериските пумпи.[3] Иако одредени транспортери изнесуваат специфичен тип на супстрати, поголемиот број изнесуваат различни класи на лекови, со значително различни хемиски структури.[17] Овие транспортери со заедничко име се нарекуваат ABC-транспортери на отпорност кон повеќе лекови (MDR — multidrug resistence), а понекогаш се нарекуваат и „хидрофобни правосмукалки“.[53]
P-гликобелковината е добро проучена белковина која придонесува на отпорноста на клетката кон повеќе лекови. Тој припаѓа на човечката ABCB (MDR/TAP)-семејство, а исто така е познат како ABCB1 или MDR1 Pgp. MDR1 се состои од функционален мономер со два трансмембрански домена (TMD) и два домена за врзување на нуклеотиди (NBD). Оваа белковина главно може да транспортира катјонски или електрично-неутрални супстрати, како и широк спектар на амфифилни супстрати. Структурата на целиот ABCB1-мономер е добиена во присуство и во отсуство на нуклеотиди, со користење на електронска крио-кристалографија. Без врзани нуклеотиди, TMD се приближно паралелни и формираат сноп кој ја опкружува централната пора, со отвор кон вонклеточната страна на мембраната. Во присуство на нехидролизирачкиот ATP-аналог, AMP-PNP, TM-домените значително се реорганизирани, со три јасно одделени домени. Централната пора, која е опкружена со TM-домените, делумно е отворена кон внатреклеточната страна на клетката, со простор помеѓу двата домена кој овозможува пристап на супстратот од липидната фаза. Значителната промена во пакувањето и можната ротација на TM-завојниците по врзувањето на нуклеотидите сугерираат дека механизмот на транспорт е преку ротација на завојниците.[17]
Геномот на растението Arabidopsis thaliana кодира 120 ABC белковини, за разлика од човечкиот геном и геномот на винската мушичка (Drosophila melanogaster) кои кодираат 50-70 ABC-белковини. Растителните ABC-белковини се поделени во 13 потсемејства врз основа на големината (полн, половичен или четврт), орентацијата и севкупната сличност во аминокиселинската низа.[62] Хомолозите на отпорност кон повеќе лекови (MDR), исто така познати и како P-гликобелковини, претставуваат најголемото потсемејство кај растенијата со 22 члена и второ по големина ABC-потсемејство. Потсемејството B на растителните ABC-транспортери (ABCB) се состои од белковини кои се одликувани по нивната локализација на плазматската мембрана.[63] Растителните ABCB-транспортери се одликуваат со хетерологна експресија во E. coli, S. cerevisiae, Schizosaccharomyces pombe и HeLa-клетки за да се утврди супстратната специфичност. Откриено е дека растителните ABCB-транспортери го транспортираат фитохормонот индол-3-оцетна киселина, исто така познат како ауксин, кој е значаен регулатор на растот и развојот на растенијата.[64][65][66] Насочениот, поларен транспорт на ауксинот посредува во растителните одговори на стимулансите од околината, по пат на процеси како што се фототропизмот и гравитотропизмот.[67] Други ABCB транспортери, како што е ABCB4, учествуваат и во изнесувањето и во внесувањето на ауксинот во клетката.[65] При ниски внатрешноклеточни концентрации на ауксин, ABCB4 игра улога на импортер на ауксин, сè додека неговата концентрација не достигне одредено ниво. Кога концентрацијата на ауксин во клетката ќе го надмине тоа ниво, ABCB4 ја менува својата функција во извозник на ауксин, регулирајќи ја на тој начин неговата концентрација во клетката.[65][68]
Првата објавена високорезолуциска структура на ABC-извозник била онаа на Sav1866 од S. аureus.[17][69] Sav1866 е хомолог на ABC-транспортери кои транспортираат повеќе лекови. Тој покажува значителна сличност во низата со човечките ABC-транспортери од потсемејството B, вклучувајќи ги MDR1 и TAP1/TAP2. Познато е дека ATPазната активност на Sav1866 е стимулирана од антиканцерогени лекови, како што се доксорубицин, винбластин и други.[70] Ова укажува на слична супстратна специфичност со P-гликобелковината и, според тоа, можен заеднички механизам за транслокација на супстрат. Sav1866 е хомодимер на половични транспортери и секоја подединица содржи N-терминален TMD со шест завојници и С-терминален NBD. NB-домените се слични по структура со оние на другите ABC-транспортери, кај кои двете ATP-врзувачки места се формираат на димерниот интерфејс помеѓу Вокеровиот А-мотив од едниот NBD и LSGGQ мотивот од другиот NBD. Структурата на Sav1866 со врзани ADP покажува дека NBD се во затворен димер и дека ТМ-завојниците се разделени со две „крила“ ориентирани кон периплазмата, со што формираат конфигурација која е отворена кон надворешната страна. Секое „крило“ се состои од завојниците ТМ1-2 од едната подединица и ТМ3-6 од другата подединица. Транспортерот содржи долги внатрешноклеточни петелки (ICL или ICD) кои ги поврзуваат ТМ-домените и кои се протегаат далеку од липидниот двослој во цитоплазмата. Додека увозниците содржат кратка спрегнувачка завојница кој е во контакт со еден NBD, Sav1866 има два внатреклеточни спрегнувачки завојници, од кои едниот (ICL1) е во контакт со NB-домените на двете подединици, а другиот (ICL2) формира заемодејства само со спротивната NBD-подединица.[21][24][52]
MsbA е ABC-транспортер на отпорност кон повеќе лекови (MDR), а можно е да претставува и липидна флипаза. Станува збор за ATPаза која го транспортира липидот А, кој е хидрофобниот дел на липополисахаридите (LPS) и е сахаролипид заснован на гликозамин, а го гради надворешниот монослој на надворешните мембрани на повеќето Грам-негативни бактерии. Липидот А е ендотоксин, па затоа губењето на MsbA од клеточната мембрана или негова мутација која предизвикува пореметување на транспортот доведува до смрт на бактериската клетка. Оваа белковина е блиску хомологна со P-белковината (Pgp) во поглед на низата и има сродна супстратна специфичност со MDR-ABC-транспортерот LmrA од Lactococcus lactis.[71] MsbA од E. coli е 36 % идентичен со N-терминалната половина на човечкиот MDR1, што сугерира дека имаат ист механизам на транспорт на амфифатични и хидрофобни супстрати. MsbA генот кодира половичен транспортер кој се состои од трансмембрански домен (TMD) споен со доменот за врзување на нуклеотиди (NBD). MsbA е хомодимер со тотална молекулска маса од 129,2 kD. Тој содржи шест ТМ-домени на периплазматската страна, еден NB домен сместен на цитоплазматската страна од клеточната мембрана и внатреклеточен домен (ICD) кој ги премостува TMD и NBD. Сочуваната завојница, која се протега од TMD сегментот до активното место на NBD, во голема мера е одговорна за преносот на информации меѓу TMD и NBD. Специфична ICD1 служи како сочувана стационарна точка околу која NBD може да ротира, што овозможува дисоцијација и димеризација на NBD во тек на врзувањето и хидролизата на ATP.[3][14][17][21][42][52][53][72]

Претходно објавените (сега повлечени) кристални структури на MsbA биле недоследни со бактерискиот хомолог Sav1866.[73][73] Структурите биле преиспитани и било утврдено дека содржат грешка и дека поради тоа моделите на MsbA биле неточни. Неодамна, овие грешки биле коригирани и биле објавени нови структури.[39] Во состојба на мирување MsbA на E. coli има форма на превртена буква „V“, со комора која е достапна од внатрешната страна на транспортерот. Контактите на димерот се концентрирани во регионот на вонклеточните петелки и додека NB-домените се на растојани од приближно 50 Å, подединиците на димерот се наоѓаат една наспроти друга. Растојанието помеѓу аминокиселинските остатоци на местото на димерниот интерфејс е утврдено со помош на експерименти на вкрстено врзување[74] и со EPR (електронска парамагнетна резонанца).[75] Релативно големата комора овозможува транспорт на големи молекулски групи, како оние присутни во липидот А. Потребни се значителни конформациони промени за да се пренесат големи шеќерни групи низ мембраната. Разликата меѓу двете структури без врзани нуклеотиди (апо) е приближно 30° придвижување на ТМ4/ТМ5 завојниците во однос на ТМ3/ТМ6 завојниците. Кај MsbA од V. cholerae, во затворената апо состојба, NB домените се порамнети и, иако се доближени, тие не формираат ATP-сендвич, а P-петелките на спротивните мономери се сместени една покрај друга. Во споредба со отворената конформација, димерниот интерфејс на ТМ-домените во затворена конформација со лицето кон внатре има екстензивни контакти. И кај двете апо конформации на MsbA, отворот на комората е од внатрешната страна. Структурата на MsbA-AMP-PNP (5’-аденилил-β-γ-имидофосфат) од S. typhimurium е слична со Sav1866. NB-домените во конформацијата со врзани нуклеотиди и лице кон надворешната страна заедно формираат канонски ATP димерен сендвич, т.е. нуклеотидот е сместен меѓу P-петелката и LSGGQ мотивот. Конформационата транзиција од MsbA-затворена-апо до MsbA-AMP-PNP опфаќа два чекори: приближно 10° придвижување на ТМ4/TM5 завојниците кон ТМ3/ТМ6, приближување на NB домените, но не и нивно порамнување, по што следи свртување на ТМ4/ТМ5 завојниците за приближно 20° надвор од рамнината. Свртувањето резултира со сепарација на ТМ3/ТМ6 завојниците од ТМ1/ТМ2 завојниците, што доведува до промена од конформација со отвор кон внатре во конформација со отвор кон надвор. Според тоа, промените во ориентацијата и растојанието на NB домените драматично го реаранжираат пакувањето на трансмембранските завојници и делотворно го менуваат пристапот на комората од внатрешноста на мембраната во пристап од надворешноста на мембраната.[39] Структурите добиени за MsbA се основа за транспортниот модел по пат на свртување.[17] Опишаните структури исто така ја нагласуваат динамичката природа на ABC извозниците, што е потврдено и со флуоресцентни и со EPR-истражувања.[52][75][76] Во најново време откриени се и инхибитори на MsbA.[77][78]

ABC-извозниците имаат транспортен механизам кој е доследен и со моделот на наизменичен пристап и со моделот на ATP-прекинувач. Во апо состојбата на извозниците, конформацијата е насочена кон внатрешноста, а TMD и NBD се релативно оддалечени едни од други за да можат да примаат амфифилни или хидрофобни супстрати. На пример, кај MsbA транспортерот големината на комората е соодветна за сместување на големи шеќерни групи од липополисахаридите (LPS). Како што е докажано од повеќе истражувачки тимови, врзувањето на супстратот е она што го покренува целиот транспортен циклус. Врзувањето на ATP, кое ја индуцира димеризацијата на NBD и формирањето на ATP-сендвичот, е она што ги покренува конформационите промени во TMD. Покажано е дека кај MsbA-шеќерните групи влегуваат во комората за време на врзувањето на ATP. Комората на MsbA е исполнета со остатоците на поларни и наелектризирани аминокиселини, што создава енергетски неповолна средина за хидрофобни супстрати, но енергетски поволна средина за поларните шеќерни групи на LPS. Бидејќи липидот не може долго време да биде стабилен во средината на комората, тој се „превртува“ и влегува во надворешниот липиден слој од мембраната. Ова „превртување“ може да биде поттикнато и од спуштањето на цврстите тела на ТМ-доменот додека хидрофобните „опашки“ на LPS молекулата се провлекуваат низ липидниот двослој. Со препакување на завојниците конформацијата на белковината се менува во состојба во која отворот е насочен кон надворешноста. Хидролизата на ATP може да го прошири периплазматскиот отвор и да го поттурне супстратот кон надворешниот слој на липидниот двослој. Со хидролиза на другата ATP-молекула и ослободувањето на ADP и Pi, NB домените се одвојуваат, по што следи враќање во состојбата на мирување и отворање на комората кон цитоплазмата.[39][42][50][53][73][73][75][79]
Познато е дека ABC-транспортерите имаат клучна улога во развивањето на отпорноста кон повеќе лекови (MDR, од анг. MultiDrug Resistence). Во случаите на MDR, пациентите кои користат лекови развиваат отпорност не само на лекот кој го примаат, туку и на неколку различни типови на лекови. Ваквата отпорност е предизвикана од повеќе фактори, а еден од нив е зголеменото излачување на лекот од клетките со посредство на ABC-транспортерите. На пример, ABCB1-белковината (P-белковината) ги изнесува тумор-супресорните лекови од клетката. P-белковината (наречен и MDR1, ABCB1, Pgp) е прототип на ABC-транспортерите и е најекстензивно проучуваниот ген од тоа семејство. Познато е дека Pgp транспортира органски катјонски и неутрални молекули. За неколку членови на ABCC семејството (познати и како MRP) познато е дека имаат MDR дејство на органски анјонски соединенија. Најдобро проучен член на ABCG семејството е ABCG2, исто така познат како BCRP (од анг. Breast Cancer Resistence Protein – белковина на отпорност на рак на дојка), кој создава отпорност на повеќето инхибитори на топоизомераза I и II, како што се топотекан, иринотекан и доксорубицин.
Сè уште не е објаснето како овие белковини можат да транслоцираат толку многу лекови кои драстично се разликуваат во нивната хемиска структура, но еден од моделите (моделот на хидрофобна правосмукалка) предлага дека сите овие лекови се врзуваат за P-белковината на основа на нивната хидрофобност.
Откритието на првите еукариотски ABC-транспортери се случило за време на истражувања на култури од клетки и туморски клетки кои покажувале отпорност кон повеќе лекови со различни хемиски структури. Било покажано дека овие клетки имаат висока експресија на транспортна белковина на отпорност кон повеќе лекови (MDR), кој првично бил наречен P-гликобелковина (Pgp), а подоцна станал познат и како MDR1 (од анг. MultiDrug Resistence protein 1) или ABCB1. Како и сите други ABC-транспортери така и овој користи хидролиза на ATP за да експортира голем вариетет на хемиски соединенија (лекови) од цитозолот во вонклеточната течност. Во клетките кои се отпорни кон повеќе лекови доаѓа до прекумерна продукција на MDR1-белковината поради високата активност на MDR1 генот. Супстрати на MDR1 кај цицачите се главно планарни, липосолубилни молекули со еден или повеќе позитивни полнежи. Повеќето лекови кои MDR1 ги изнесува надвор од цитозолот се мали, неполарни молекули, кои лесно можат да дифундираат од вонклеточниот медиум во цитозолот, каде тие блокираат различни клеточни функции. Лековите како колхицин и винбластин, кои ја блокираат интеграцијата на микротубулите, слободно ја преминуваат клеточната мембрана и навлегуваат во цитозолот, но активноста на MDR1 ја намалува нивната концентрација во клетката. Поради тоа, за да се убијат клетките кои вршат експресија на MDR1 генот потребни се повисоки концентрации на лекот во споредба со оние клетки кои не вршат експресија на овој ген.[9]
Други ABC-транспортери кои создаваат резистенција кон повеќе лекови се ABCC1 (MRP1) и ABCG2 (анг. Breast Cancer Resistence Protein).[80]
За да се реши проблемот на отпорност кон повеќе лекови создадена од MDR1, можат да се користат различни типови на лекови или инхибитори на ABC-транспортерите. Овие типови на лекови треба да поседуваат способност да го избегнат транспортот на MDR1. Ваква способност имаат алкилирачките лекови (циклофосфамид), антиметаболити (5-флуороурацил) и антрациклинските изменети лекови (анамицин и доксорубицин-пептид). Сите тие не се супстрати на ABC-транспортерите, па затоа не можат да бидат исфрлени од клетката. Друга можност е да се користи комбинација на ABC инхибитори и антиканцероген лек истовремено.
Отпорноста на лекови е чест клинички проблем кој се јавува кај пациенти заболени од инфективни болести и кај пациентите кои страдаат од рак. Прокариотските и еукариотските микроорганизми, како и неопластичните клетки, често се отпорни на лекови. MDR често е поврзан со прекумерна експресија на ABC-транспортерите. Инхибицијата на ABC-транспортерите со соединенија со ниска молекулска маса била екстензивно испитувана кај пациентите заболени од рак; сепак, клиничките резултати биле разочарувачки. Неодамна беа применети разни РНКi стратегии за да се анулира отпорноста во различни типови на тумори и утврдено е дека оваа технологија е ефикасна во поништувањето на отпорноста која е посредувана од ABC-транспортерите во клетките на ракот, па затоа оваа стратегија се смета за ветувачка во надминување на отпорноста со употреба на генетските терапевтици. Примената на РНКi технологијата, исто така, има потенцијал за надминување на отпорноста во третманите на инфективните заболувања предизвикани од микробиолошки патогени.[81]
Физиолошката улога на ABC-транспортерите е изразена во мембраната на здравите клетки, каде тие го посредуваат транспортот на разни ендогени супстанци, како и на низа други супстанци кои се страни за организмот. На пример, ABC-транспортерите, како што се Pgp, MRPs и BCRP, ја ограничуваат апсорпцијата на многу лекови во дигестивниот систем и ги отстрануваат лековите од клетките на црниот дроб во жолчката,[82] како механизам за отстранување на страните супстанци од телото. Голем број на лекови или се транспортирани од самите ABC-транспортери или влијаат на транспортот на другите лекови преку тие транспортери. Второто сценарио може да доведе до заемодејства меѓу лековите,[83] кои понекогаш резултираат со промени во дејството на лековите.[84]
Постојат неколку типови на тестови кои овозможуваат детекција на интеракција на ABC-транспортери со ендогени и ксенобиотични соединенија.[85] Комплексноста на тестовите се движи во рамки од релативно едноставни мембрански анализи,[86] како што е тестот на везикуларниот транспорт, ATPазниот тест, до посложени клеточни тестови и доста сложени in vivo детекциони методи.[87]
Везикуларниот транспортен тест ја детектира транслокацијата на молекулите преку ABC-транспортерите.[88] Мембраните подготвени под соодветни услови содржат обратно-ориентирани везикули на места на врзување на ATP и на места на врзување на супстратот на транспортерот на надворешната страна. Везикулите го преземаат супстратот на транспортерот на начин кој зависи од ATP. Брза филтрирација со користење на филтри со стаклени влакна или нитроцелулозни мембрани се користи за одвојување на везикулите од инкубациониот раствор, при што тестираното соединение заробено внатре во везикулата се задржува на филтерот. Количината на транспортираните необележани молекули се определува со помош на HPLC, LC/MS, LC/MS/MS. Алтернативно, соединенијата можат да се обележат со радиоактивни или флуоресцентни ознаки, така што радиоактивноста или флуоресценцијата која се задржува на филтерот може да се квантифицира.
Во везикуларните транспортни студии се користат различни типови на мембрани од различни извори (на пример, клетки на инсекти, трансфецирани или одбрани клеточни линии на цицачи). Мембраните се комерцијално достапни или можат да бидат подготвени од различни клетки, па дури и ткива, на пр. црнодробни каналикуларни мембрани. Овој тип на тест има предност во мерењето на вистинската диспозиција на супстратот низ клеточната мембрана. Неговиот недостаток е што соединенијата со средна до висока пасивна пермеабилност не се задржуваат во внатрешноста на везикулата, што прави да директните мерења на транспортот се тешко изводливи.
Тестот на везикуларниот транспорт може да биде изведен на индиректен начин, така што тестираните лекови кои стапуваат во интеракција ја модулираат брзината на транспортот на соединението-гласник. Таков тип на тестови е посебно погоден за детекција на можни заемодејства помеѓу лекови и интеракција на лекови со ендогени супстрати. Овие тестови не се осетливи на пасивна пермеабилност на соединенијата и затоа ги детектираат сите соединенија кои стапуваат во интеракција. Овој тип на тестови не обезбедува информации за тоа дали тестираното соединение е инхибитор на транспортерот, или супстратот ја инхибира функцијата на транспортерот на компетитивен начин. Типичен пример за индиректен везикуларен транспортен тест е детекција на инхибиција на таурохолатен транспорт со посредство на ABCB11 (BSEP).
Клетките кои вршат експресија на ефлуксни транспортери активно пумпаат супстрати надвор од клетката, што доведува до снижување на брзината на акумулација на супстратот, до пониски внатреклеточни концентрации во тек на стационарната состојба, или до зголемена брзина на елиминација на супстратот од клетки заситени со супстрат. Транспортираните радиоактивни супстрати или обележаните флуоресцентни бои можат директно да се измерат, а на индиректен начин модулацијата на акумулацијата на пробниот супстрат (на пр. флуоресцентни бои како родамин 123 или калцеин) може да се одреди во присуство на тестираниот лек.[83]
Калцеинот-АМ, е високопермеабилен дериват на калцеинот и затоа лесно влегува во неоштетена клетка, каде ендогените естерази брзо го хидролизираат до флуоресцентен калцеин. За разлика од калцеинот-АМ, калцеинот има ниска пермеабилност, поради што е заробен во клетките и поради тоа се акумулира. Бидејќи калцеинот-АМ е одличен супстрат на МDR1 и MRP1 ефлукс-транспортерите, клетките кои вршат експресија на MDR1 и/или MRP1 транспортерите го исфрлаат калцеинот-AM од клетките, пред тој да може да биде хидролизиран од естеразите. Ова резултира со пониска клеточна акумулација на калцеинот. Колку е поголема активноста на MDR во клеточната мембрана, толку помалку калцеинот се акумулира во цитоплазмата. Во клетките кои вршат експресија на MDR, додавањето на MDR инхибиторот, или пак на вишок на MDR супстрат, драматично ја зголемува брзината на акумулација на калцеинот. Активноста на транспортерите на отпорност кон повеќе лекови се одразува како разлика помеѓу количината на бојата акумулирана во присуството или во отсуството на инхибиторот. Со користење на селективни инхибитори може да се забележи разлика меѓу транспортната активност на MDR1 и MRP1. Овој тест може да се користи за тестирање на лекови за транспортерски заемодејства, како и за квантификација на MDR активноста на клетките. Калцеинскиот тест е комерцијален тест на SOLVO Biotechnology.
Потсемејството ABCA е составена од 12 целосни транспортери поделени во две подгрупи. Првата подгрупа се состои од седум гени кои се мапирани на шест различни хромозоми. Тоа се ABCA1-4, ABCA7, ABCA12 и ABCA13. Другата подгрупа се состои од ABCA5-6 и ABCA8-10. Целата подгрупа 2 е организирана како еден кластер на гени на хромозомот 17q24. Гените на втората подгрупа се разликуваат од гените слични на ABCA1 по тоа што имаат 37-38 егзони, за разлика од ABCA1 кој има 50 егзони. Подгрупата ABCA1 е имплицирана за развој на повеќе генетски заболувања. Во рецесивната Тангиерова болест, ABCA1-белковината е мутирана. Исто така, ABCA4 се наоѓа во регионот на 1p21 хромозомот, кој го содржи генот за Штаргардтовата болест. Утврдено е дека овој ген е со висока експресија во стапчестите фоторецептори и е мутиран кај заболените од Штаргардтовата болест, рецесивниот ретинитисен пигментизам и кај повеќето рецесивни дистрофии на конусно-стапчестите рецептори.[8]
Потсемејството ABCB е составена од четири целосни транспортери и два полутранспортери. Тоа е единствено потсемејство кај човекот коа содржи целосни и полутипови на транспортери. Откриено е дека ABCB1 (гликобелковина на пермеабилноста, P-gp, Pgp) е белковина која е со прекумерна експресија во одделни клетки на тумори отпорни на лекови. Овој гликобелковина кај луѓето е кодиран од ABCB1 генот. Тој е првенствено изразен во крвно-мозочната бариера и во црниот дроб, а се смета дека учествува во заштитата на клетките од токсини. Клетките кои вршат прекумерна експресија на оваа белковина покажуваат отпорност на повеќе видови лекови.[8]
Потсемејството ABCC содржи тринаесет членови, а девет транспортери од оваа група се нарекуваат белковини на отпорност на повеќе видови лекови (MRP). MRP белковините се широко застапени во природата и посредуваат во мноштво важни функции.[89] Познато е дека тие учествуваат во транспортот на јони, секрецијата на токсини и во преносот на сигнали.[8] Од деветте MRP белковини, четири, MRP4, 5, 8, 9, (ABCC4, 5, 11 и 12), имаат типични ABC структури со четири домена, што опфаќа два трансмембрански домена, при што на секој од нив се надоврзува домен за врзување на нуклеотид. Тие се нарекуваат кратки MRP белковини. Останатите 5 MRP белковини, MRP1, 2, 6, 7 (ABCC1, 2, 3, 6 и 10) се познати како долги MRP белковини. Се нарекуваат „долги“ затоа што имаат дополнителен петти домен на нивниот N-крај.[89]
Како дел од ова семејство се смета и CFTR, транспортерот кој учествува во болеста цистична фиброза. Ова заболување се јавува по мутација и губење на функцијата на CFTR.[8] CFTR ги транспортира хлоридните и тиоцијанатните јони низ мембраните на епителијалните клетки. Мутацијата на овој ген влијае врз функционирањето на каналите за хлоридни јони во овие клеточни мембрани што доведува до цистична фиброза и вродено отсуство на вас деференс.
Рецепторите за сулфонилуреа (SUR), кои учествуваат во секрецијата на инсулин, во невронските и мускулните функции, исто така се дел од ова семејство на белковини. Мутацијата на SUR-белковината е потенцијална причина за неонатален дијабетес мелитус. SUR, исто така, е место за врзување на сулфонилуреа лекови и активаторите на калиумовите канали, како што е диазоксид.
Потсемејството ABCD се состои од четири гени кои кодираат полутранспортери, со експресија исклучиво во пероксизомот. ABCD1 е одговорен за X-поврзаната форма на адренолеукодистрофија (ALD). Оваа болест се одликува со невродегенерација и недостаток на адреналин, а обично се јавува во доцното детство. Во клетките на пациентите со ALD, се акумулираат неразгранети заситени масни киселини, иако улогата на ABCD1 во овој процес сè уште не е одредена. Функцијата на другите ABCD гени допрва треба да се утврди, но се верува дека вршат сродни функции во метаболизмот на масните киселини.[8]
Овие две подгрупи се состојат од гени кои имаат ATP-врзувачки домени, кои се блиску сродни со другите ABC-транспортери, иако овие гени не кодираат трансмембрански домени. ABCE има само еден член, OABP или ABCE1, за кој е познато дека препознава одредени олигодендроцити создадени како одговор на специфични вирусни инфекции. Сите членови на ABCF подгрупата се состојат од еден пар на ATP-врзувачки домени.[8]
ABCG потсемејството ја сочинуваат шест полутранспортери со ATP-врзувачки места на N-крајот и трансмембрански домени на C-крајот. Ориентацијата е спротивна кај сите други ABC гени. Постојат само 5 ABCG гени во човечкиот геном, додека во геномот на Drosophila melanogaster има 15, а во квасецот 10 гена. ABCG2 генот бил откриен во клеточните линии кои се одвоени поради високото ниво на отпорност кон митоксантрон, а кај кои отсуствува експресија на ABCB1 или ABCC1. ABCG2 може да експортира антроциклински антиканцерски лекови, како што се топотекан, митоксантрон или доксорубицин. Утврдено е дека хромозомските транслокации предизвикуваат амплификација или преуредување на ABCG2 генот присутен во отпорните клеточни линии. Нормалната функција на ABCG2 сè уште не е позната.[8]
Познати се 48 ABC-транспортери кај луѓето. Во геномската организација кај човекот тие се класифицирани во седум семејства.
| Семејство | Членови | Функција | Примери |
|---|---|---|---|
| ABCA | Ова семејство ги содржи некои од најголемите транспортери (со должина над 2.100 аминокиселини). Пет од нив се наоѓаат во кластерот на 17q24 хромозомот. | Одговорни се, меѓу другото, за транспорт на холестерол и липиди. | ABCA12 ABCA1 |
| ABCB | Ова семејство се состои од 4 целосни и 7 полутранспортери. | Некои од нив се наоѓаат во крвно–мозочната бариерата, црниот дроб и во митохондриите. Тие транспортираат пептиди и составни компоненти на жолчката. | ABCB5 |
| ABCC | Ова семејство се состои од 12 целосни транспортери. | Играат улога во транспортот на јони, во рецепторите на клеточната површина, во секрецијата на токсини. Во оваа група спаѓа CFTR-белковината, кој е причина за цистична фиброза кога е во дефицит. | ABCC6 |
| ABCD | Ова семејство се состои од 4 полутранспортери. | Играат улога во пероксизомите. | ABCD1 |
| ABCE/ABCF | Ова семејство се состои од еден ABCE и три ABCF белковини. | Тие, всушност, не се транспортери, туку само ATP-врзувачки домени кои се изведени од ABC семејството, иако немаат трансмембрански домени. Овие белковини главно ја регулираат синтезата или експресијата на белковините. | ABCE, ABCF1, ABCF2 |
| ABCG | Ова семејство се состои од 6 „реверзни“ полутранспортери, со NBF на NH3+ крајот и со ТМ на COO- крајот. | Тие транспортираат липиди, разновидни лекови, компоненти на жолчката, холестерол и други стероиди. | ABCG2 ABCG1 |
Систем за класификација на транспортери на водорастворливи супстанци:[90]
Пермеази за внесување од ABC-тип
Пермеази за ефлукс од ABC-тип (прокариотски)
ABC1:
ABC2:
ABC3:
ECF:
S-подединиците се хомологни на:
Список на белковини кои припаѓаат на ABC натсемејството : јануари 9 тука
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.