Magnezij u biologiji
From Wikipedia, the free encyclopedia
Remove ads
Magnezij je esencijalni element u biološkim sistemima. Magnezij se obično javlja kao Mg2+ ion. To je esencijalni mineralni nutrijent (tj. element) za život.[1][2][3][4] i prisutan je u svakoj vrsti ćelija i u svakom organizmu. Naprimjer, adenozin-trifosfat (ATP), glavni izvor energije u ćelijama, mora se vezati za ion magnezija da bi bio biološki aktivan. Ono što se naziva ATP često je zapravo Mg-ATP.[5] Kao takav, magnezij ima ulogu u stabilnosti svih polifosfatnih spojeva u ćelijama, uključujući i one povezane sa sintezom DNK i RNK.
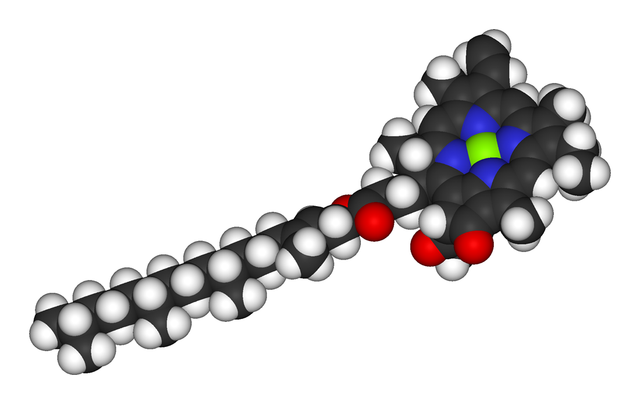
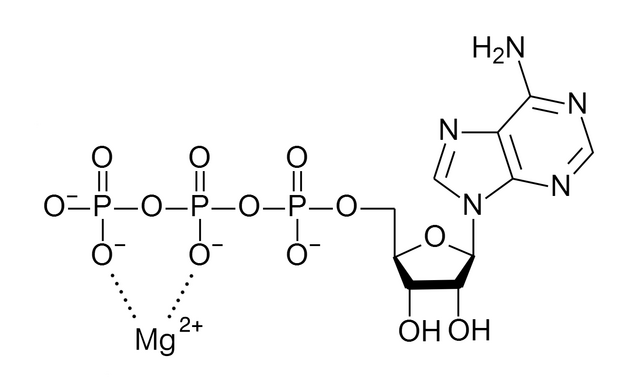
Preko 300 enzima zahtijeva prisustvo magnezijskih iona za svoje katalitsko djelovanje, uključujući sve enzime koji koriste ili sintetiziraju ATP ili one koji koriste druge nukleotide za sintezu DNK i RNK.[6]
Kod biljaka, magnezij je neophodan za sintezu hlorofila i fotosintezu.
Remove ads
Funkcija
Ravnoteža magnezija je vitalna za dobrobit svih organizama. Magnezij je relativno obilan ion u Zemljinoj kori i plaštu i visoko je bioraspoloživ u hidrosferi. Ova dostupnost, u kombinaciji s korisnom i vrlo neobičnom hemijom, možda je dovela do njegove upotrebe u evoluciji kao iona za signalizaciju, aktivaciju enzima i katalizu. Međutim, neobična priroda ionskog magnezija također je dovela do velikog izazova u upotrebi iona u biološkim sistemima. Biološke membrane su nepropusne za magnezij (i druge ione), tako da transportni proteini moraju olakšati protok magnezija, kako u, tako i iz ćelija i unutarćelijskih odjeljaka.[7]
Ljudsko zdravlje
Nedovoljan unos magnezija često uzrokuje grčeve mišića i povezan je sa kardiovaskularnim bolestima, dijabetesom,visokim krvnim pritiskom, anksioznim poremećajima, migrenom, osteoporozom i cerebralnim infarktom.[8][9] Akutni nedostatak (vidi hipomagnezemija) je rijedak i češći je kao nuspojava lijekova (kao što je hronična upotreba alkohola ili diuretika) nego od niskog unosa hrane per se, ali se može javiti kod osoba koje se hrane intravenozno duži vremenski period.
Najčešći simptom prekomjernog oralnog unosa magnezijuma je dijareja. Dodaci prehrani bazirani na aminokiselinama helatima (kao što su glicinat, lizinat itd.) mnogo se bolje podnose od strane probavnog sistema i nemaju nuspojave starijih spojeva koji se koriste, dok dodaci prehrani sa produženim oslobađanjem suplementi prehrani sprječavaju pojavu dijareje. Budući da bubrezi odraslih ljudi efikasno izlučuju višak magnezijuma, oralno trovanje magnezijumom kod odraslih sa normalnom bubrežnom funkcijom je vrlo rijetko. Dojenčad, koja imaju smanjenu sposobnost izlučivanja viška magnezija čak i kada su zdrava, ne bi trebala primati suplemente magnezija, osim pod nadzorom ljekara.
Farmaceutski preparati sa magnezijem se koriste za liječenje stanja uključujući nedostatak magnezija i hipomagnezemiju, kao i eklampsiju.[10] Takvi preparati su obično u obliku magnezij- sulfata ili hlorida kada se daju parenteralno. Magnezij se apsorbuje sa razumnom efikasnošću (30-40%) u organizmu iz bilo koje rastvorljive magnezijeve soli, kao što su hlorid ili citrat. Magnezij se slično apsorbuje iz Epsom soli, iako sulfat u ovim solima pojačava njihov laksativni efekat u većim dozama. Apsorpcija magnezija iz nerastvorljivih oksidnih i hidroksidnih soli (magnezijevog mlijeka) je nepravilna i slabije efikasnosti, jer zavisi od neutralizacije i rastvaranja soli kiselinom želuca, što možda nije (i obično nije) potpuno.
Magnezij-orotat se može koristiti kao adjuvantna terapija kod pacijenata na optimalnom liječenju teškog kongestivnog zatajenja srca, povećavajući stopu preživljavanja i poboljšavajući kliničke simptome i kvalitet života.[11]
U 2022. godini, magnezijeve soli su bile 207. najčešće propisivani lijek u Sjedinjenim Američkim Državama, sa više od milion recepata.[12][13]
Provodljivost živaca
Magnezij može uticati na opuštanje mišića direktnim djelovanjem na ćelijske membrane. Mg2+ ioni zatvaraju određene tipove kalcijskih kanala, koji provode pozitivno naelektrisane kalcij u biologiji|kalcijske ione u neurone. Sa viškom magnezija, više kanala će biti blokirano i aktivnost nervnih ćelija će se smanjiti.[14][15]
Hipertenzija
Intravenski magnezij-sulfat se koristi u liječenju preeklampsije.[16] Za hipertenziju koja nije povezana s trudnoćom, meta-analiza 22 klinička ispitivanja s rasponom doza od 120 do 973 mg/dan i prosječnom dozom od 410 mg, zaključila je da suplementacija magnezijem ima mali, ali statistički značajan učinak, snižavajući sistolni krvni pritisak za 3–4 mm Hg i dijastolni krvni pritisak za 2–3 mm Hg. Učinak je bio veći kada je doza bila veća od 370 mg/dan.[17]
Dijabetes i tolerancija glukoze
Veći unos magnezija putem ishrane odgovara nižoj incidenciji dijabetesa.[18] Za osobe s dijabetesom ili s visokim rizikom od dijabetesa, suplementacija magnezijem snižava glukozu natašte.[19]
Mitohondrije
Magnezij je neophodan kao dio procesa koji generira adenozin-trifosfat.[20][21]
Mitohondrije se često nazivaju "elektranama ćelije" jer je njihova primarna uloga generiranje energije za ćelijske procese. To postižu razgradnjom nutrijenata, prvenstveno glukoze, kroz niz hemijskih reakcija poznatih kao ćelijsko disanje. Ovaj proces na kraju proizvodi adenozin trifosfat (ATP), glavnu energetsku valutu ćelije.
Vitamin D
Magnezij i vitamin D imaju sinergijski odnos u tijelu, radeći zajedno kako bi optimizirali međusobne funkcije.[22][23]
Testosteron
Teoretizira se da je za pravilno funkcioniranje procesa stvaranja testosterona iz holesterola potreban magnezij.[21]
Studije su pokazale da značajno povećanje testosterona nastaje nakon uzimanja 10 mg magnezija/kg tjelesne težine/dan.[24]
Remove ads
Preporuke za ishranu
Američki institut za medicinu (IOM) ažurirao je 1997. godine Procijenjene prosječne potrebe (EAR) i Preporučene prehrambene doze (RDA) za magnezij. Ako nema dovoljno informacija za utvrđivanje EAR i RDA, umjesto toga se koristi procjena nazvana Adekvatan unos (AI). Trenutne EAR za magnezij za žene i muškarce starosti 31 i više godina su 265 mg/dan i 350 mg/dan. RDA su 320 i 420 mg/dan. RDA su veće od EAR kako bi se identifikovale količine koje će pokriti osobe sa višim od prosječnih potreba. RDA za trudnoću je 350 do 400 mg/dan, ovisno o dobi žene. RDA za dojenje se kreće od 310 do 360 mg/dan iz istog razloga. Za djecu uzrasta od 1 do 13 godina, preporučeni dnevni unos (RDA) se povećava s godinama od 65 do 200 mg/dan. Što se tiče sigurnosti, IOM također postavlja gornju dozvoljenu dozu unosa (UL) za vitamine i minerale kada postoje dovoljni dokazi. U slučaju magnezija, gornja dozvoljena doza je postavljena na 350 mg/dan. Gornja dozvoljena doza je specifična za magnezij koji se konzumira kao dodatak prehrani, a razlog tome je što previše magnezija konzumiranog odjednom može uzrokovati proljev. Gornja dozvoljena doza se ne odnosi na magnezij iz hrane. Zajedno, preporučeni dnevni unos (EAR), RDA i UL se nazivaju referentnim dnevnim unosom (Dietary Reference Intake).[25]
* = Adekvatan unos
Evropska agencija za sigurnost hrane (EFSA) naziva kolektivni skup informacija Dijetetskim referentnim vrijednostima, s referentnim unosom populacije (PRI) umjesto RDA i prosječnim potrebama umjesto EAR. AI i UL definirani su isto kao u Sjedinjenim Američkim Državama. Za žene i muškarce starije od 18 godina, AI su postavljeni na 300 i 350 mg/dan. AI za trudnoću i dojenje također su 300 mg/dan. Za djecu uzrasta 1-17 godina, AI se povećavaju s godinama od 170 do 250 mg/dan. Ovi AI su niži od američkih RDA.[27] The European Food Safety Authority reviewed the same safety question and set its UL at 250 mg/day – lower than the U.S. value.[28] Gornja granica unosa magnezijuma (UL) je jedinstvena po tome što je niža od nekih preporučenih dnevnih unosa (RDA). Odnosi se samo na unos iz farmakološkog sredstva ili dodatka prehrani i ne uključuje unos iz hrane i vode.
Označavanje
Za potrebe označavanja hrane i dodataka prehrani u SAD-u, količina u porciji izražava se kao postotak dnevne vrijednosti (%DV). Za potrebe označavanje magnezija, 100% dnevne vrijednosti bilo je 400 mg, ali od 27. maja 2016. godine revidirano je na 420 mg kako bi se uskladilo s RDA.[29][30] Tabela starih i novih preporučenih dnevnih vrijednosti za odrasle dostupna je na Referentni dnevni unos.
Remove ads
Izvori hrane

Zeleno povrće poput špinata osigurava magnezij zbog obilja molekula hlorofila, koje sadrže ovaj ion. Orašasti plodovi (posebno brazilski orah, indijski orah i badem), sjemenke (npr. sjemenke bundeve), tamna čokolada, pržena soja, mekinje i neke cijele žitarice također su dobri izvori magnezija.[31]
Iako mnoge namirnice sadrže magnezij, on se obično nalazi u niskim nivoima. Kao i kod većine nutrijenata, dnevne potrebe za magnezijem vjerovatno se neće zadovoljiti jednom porcijom bilo koje pojedinačne namirnice. Konzumiranje raznovrsnog voća, povrća i žitarica pomoći će u osiguravanju adekvatnog unosa magnezija.
Budući da se magnezij lako rastvara u vodi, rafinirana hrana, koja se često prerađuje ili kuha u vodi i suši, općenito je loš izvor ovog nutrijenta. Na primjer, integralni kruh ima dvostruko više magnezija od bijelog kruha jer se klice i mekinje bogate magnezijem uklanjaju kada se bijelo brašno prerađuje. Tabela izvora magnezija u hrani sugerira mnoge prehrambene izvore magnezija.
"Tvrda" voda također može osigurati magnezij, ali "mehka" voda sadrži manje ovog iona. Istraživanja prehrane ne procjenjuju unos magnezija iz vode, što može dovesti do potcjenjivanja ukupnog unosa magnezija i njegove varijabilnosti.
Previše magnezija može otežati tijelu apsorpciju kalcija. Nedovoljno magnezija može dovesti do hipomagnezemije] kao što je gore opisano, sa nepravilnim otkucajima srca, visokim krvnim pritiskom (znak kod ljudi, ali ne i kod nekih eksperimentalnih životinja poput glodara), nesanicom i grčevima mišića (fascikulacija). Međutim, kao što je navedeno, smatra se da su simptomi niskog magnezija zbog čistog nedostatka u ishrani rijetki. U nastavku su navedene neke namirnice i količina magnezija u njima:[32]
- Sjemenke bundeve, bez ljuske (1/4 šolje) = 303 mg
- Sjemenke čia, {1/4 šolje)= 162 mg[33]
- Heljdino brašno (1/2 šolje) = 151 mg
- Brazilski orah (1/4 šolje) = 125 mg
- Zobene mekinje, sirove (1/2 šolje) = 110 mg
- Kakao prah (1/4 šolje) = 107 mg
- Halibut (3 oz) = 103 mg
- Bademi (1/4 šolje) = 99 mg
- Indijski orah (1/4 šolje) = 89 mg
- Integralno pšenično brašno (1/2 šolje) = 83 mg
- Špinat, kuhani (1/2 šolje) = 79 mg
- Blitva, kuhana (1/2 šolje) = 75 mg
- Čokolada, 70% kakao (1 oz) = 73 mg
- Tofu, čvrsti (1/2 šolje) = 73 mg
- Crni grah, kuhani (1/2 šolje) = 60 mg
- Kvinoa, kuhana (1/2 šolje) = 59 mg
- Puter od kikirikija (2 supene kašike) = 50 mg
- Orasi (1/4 šolje) = 46 mg
- Sjeme suncokretas, oljušteno (1/4 šolje) = 41 mg
- Slanutak, kuhano (1/2 šolje) = 39 mg
- Kale, kuhano (1/2 šolje) = 37 mg
- Sočivo, kuhano (1/2 šolje) = 36 mg
- Ovsene pahuljice, kuhane (1/2 šolje) = 32 mg
- Riblji sos (1 supena kašika) = 32 mg
- Mlijeko, bez masti (1 šolja) = 27 mg
- Kahva, espreso (1 oz) = 24 mg
- Hljeb od cijelog pšeničnog zrna (1 kriška) = 23 mg
Remove ads
Biološki raspon, distribucija i regulacija
Kod životinja je pokazano da različite vrste ćelija održavaju različite koncentracije magnezija.[34][35][36][37] Čini se vjerovatnim da isto važi i za biljke.[38][39] Ovo ukazuje na to da različite vrste ćelija mogu regulisati dotok i odtok magnezija na različite načine, na osnovu svojih jedinstvenih metaboličkih potreba. Intersticijske i sistemske koncentracije slobodnog magnezija moraju se delikatno održavati kombinovanim procesima puferovanja (vezivanje iona za proteine i druge molekule) i prigušivanja (transport iona u skladišne ili vanćelijske prostore).[40]). Kod biljaka, a u novije vrijeme i kod životinja, magnezij je prepoznat kao važan signalni ion, koji aktivira i posreduje u mnogim biohemijskim reakcijama. Najbolji primjer za to je možda regulacija fiksacije ugljika u hloroplastima u Calvinovom ciklusu.[41][42]
Magnezij je veoma važan za ćelijske funkcije. Nedostatak ovog nutrijent a uzrokuje bolest pogođenog organizma. Kod jednoćelijskih organizama kao što su bakterije i kvasci, nizak nivo magnezija se manifestuje znatno smanjenom stopom rasta. Kod sojeva bakterija koji transportuju magnezij nokautirajuće, zdrave stope rasta se održavaju samo uz izlaganje vrlo visokim vanjskim koncentracijama ovog iona.[43][44] Kod kvasca, nedostatak magnezija u mitohondrijama također dovodi do bolesti.[45]
Biljke kojima nedostaje magnezija pokazuju reakcije na stres. Prvi uočljivi znaci i gladovanja magnezijem i prekomjerne izloženosti magneziju kod biljaka su smanjenje brzine fotosinteze. To je zbog centralnog položaja Mg2+ iona u molekuli hlorofila. Kasniji efekti nedostatka magnezija na biljke su značajno smanjenje rasta i reproduktivne održivosti.[4] Magnezij također može biti toksičan za biljke, iako se to obično vidi samo u uslovima suša.[46][47]

Kod životinja, nedostatak magnezija (hipomagnezemija) se javlja kada je dostupnost magnezija u okolišu niska. Kod preživara, posebno osjetljivih na dostupnost magnezija u pašnjačkim travama, stanje je poznato kao 'travna tetanija'. Hipomagnezemija se prepoznaje po gubitku ravnoteže zbog slabosti mišića.[48] A number of genetically attributable hypomagnesemia disorders have also been identified in humans.[49][50][51][52] Prekomjerna izloženost magneziju može biti toksična za pojedinačne ćelije, iako je te efekte bilo teško eksperimentalno pokazati. Hipermagnezemija, prekomjerna količina magnezijuma u krvi, obično je uzrokovana gubitkom bubrežne funkcije. Zdrave životinje brzo izlučuju višak magnezija putem urina i stolice.[53] Magnezij u urinu se naziva magnezurija. Karakteristične koncentracije magnezija u modelnim organizmima su: u E. coli 30–100 mM (vezan), 0.01–1 mM (slobodan), u pupajućem kvascu 50 mM, u sisarskoj ćeliji 10 mM (vezan), 0,5 mM (slobodan) i u krvnoj plazmi 1 mM.[54]
Remove ads
Biološka hemija
Mg2+ je četvrti najzastupljeniji metalni ion u ćelijama (po molu) i najzastupljeniji slobodni dvovalentni kation – kao rezultat toga, duboko je i suštinski utkan u ćelijski metabolizam. Zaista, Mg2+-zavisni enzimi pojavljuju se u gotovo svakom metaboličkom putu: specifično vezivanje Mg2+ za biološke membrane se često uočava, Mg2+ se također koristi kao signalna molekula, a veliki dio biohemije nukleinskih kiselina zahtijeva Mg2+, uključujući sve reakcije koje zahtijevaju oslobađanje energije iz ATP-a.[55][56][42] U nukleotidima, trofosfatni dio spoja je neizbježno stabiliziran povezivanjem s Mg2+ u svim enzimskim procesima.
Hlorofil
U fotosintetskim organizmima, Mg2+ ima dodatnu vitalnu ulogu kao koordinirajući ion u molekuli hlorofila. Ovu ulogu je otkrio Richard Willstätter, koji je dobio Nobelovu nagradu za hemiju 1915. za pročišćavanje i strukturu vezivanja hlorofila sa šestim brojem ugljika.
Enzimi
Hemija Mg2+ iona, primijenjena na enzime, koristi cijeli spektar neobične reakcijske hemije ovog iona za ispunjavanje niza funkcija.[55][57][58][59] Mg2+ interaguje sa supstratima, enzimima, a povremeno i sa oba (Mg2+ može biti dio aktivnog mjesta). Općenito, Mg2+ interaguje sa supstratima putem koordinacije unutrašnje sfere, stabilizirajući anione ili reaktivne međuprodukte, uključujući i vezivanje za ATP i aktiviranje molekule za nukleofilni napad. Prilikom interakcije sa enzimima i drugim proteinima, Mg2+ se može vezati koristeći koordinaciju unutrašnje sfere, kako bi promijenio konformaciju enzima ili učestvovao u hemiji katalitičke reakcije. U oba slučaja, budući da je Mg2+ samo rijetko potpuno dehidriran tokom vezivanja liganda, možda je važna molekula vode povezana sa Mg2+, a ne sam ion. Lewisova kiselost Mg2+ (pKa 11,4) se koristi da omogući reakcije hidrolize i kondenzacije (najčešće su hidroliza fosfatnog estera i prijenos fosforila) koje bi inače zahtijevale pH vrijednosti znatno drugačije od fizioloških vrijednosti.
Bitna uloga u biološkoj aktivnosti ATP-a
ATP (adenozin trifosfat), glavni izvor energije u ćelijama, mora biti vezan za magnezijev ion da bi bio biološki aktivan. Ono što se naziva ATP često je zapravo Mg-ATP.[5]
Nukleinske kiseline
Nukleinske kiseline imaju važan raspon interakcija s Mg2+. Vezivanje Mg2+ za DNK i RNK stabilizuje strukturu; to se može uočiti u povećanoj temperaturi topljenja (Tm) dvolančane DNK u prisustvu Mg2+.[55] Osim toga, ribosomi sadrže velike količine Mg2+ i osigurana stabilizacija je neophodna za kompleksiranje ovog ribo-proteina.[60] Veliki broj enzima uključenih u biohemiju nukleinskih kiselina veže Mg2+ za aktivnost, koristeći ion i za aktivaciju i za katalizu. Konačno, autokataliza mnogih ribozima (enzima koji sadrže samo RNK) je zavisna od Mg2+ (npr. introni mitohondrijske grupe II kvasca koji se sami spajaju.[61]). Magnezijevi ioni mogu biti ključni za održavanje integriteta položaja blisko grupisanih fosfatnih grupa. Ovi klasteri se pojavljuju u brojnim i različitim dijelovima ćelijskog jedra i citoplazme. Naprimjer, heksahidratizirani Mg2+ ioni se vežu u duboki glavni žlijeb DNK i na vanjskim ustima A-oblika nukleinske kiseline dupleksi.[62]
Ćelijske membrane i zidovi
Biološke ćelijske membrane i ćelijski zidovi su polianionske površine. Ovo ima važne implikacije za transport iona, posebno zato što je pokazano da različite membrane preferencijalno vezuju različite ione.[55] I Mg2+ i Ca2+ redovno stabilizuju membrane umrežavanjem karboksiliranih i fosforiliranih glavnih grupa lipida. Međutim, pokazano je da i membrana ovojnice E. coli veže Na+, K+, Mn2+ i Fe3+. Transport iona zavisi i od gradijenta koncentracije iona i od električnog potencijala (ΔΨ) kroz membranu, na koji će uticati naboj na površini membrane. Naprimjer, specifično vezivanje Mg2+ za omotač hloroplasta implicirano je u gubitku fotosintetske efikasnosti blokadom unosa K+ i naknadnom acidifikacijom strome hloroplasta.[41]
Proteini
Mg2+ ion se obično slabo veže za proteine (Ka ≤ 105[55]) i to ćelija može iskoristiti za uključivanje i isključivanje enzimske aktivnosti, promjenama u lokalnoj koncentraciji Mg2+.Iako je koncentracija slobodnog citoplazmatskog Mg2+ reda veličine 1 mmol/L, ukupni sadržaj Mg2+ u životinjskim ćelijama je 30 mmol/L[63] a kod biljaka je sadržaj endodermalnih ćelija lista izmjeren na vrijednostima i do 100 mmol/L (Stelzer et al., 1990), od kojih je većina puferovana u odjeljcima za skladištenje. Citoplazmatska koncentracija slobodnog Mg2+ je puferovana vezivanjem za helatore (npr. ATP), ali također, što je još važnije, puferovana je skladištenjem Mg2+ u unutarćelijskim odjeljcima.[nedostaje referenca] Transport Mg2+ između unutarćelijskih odjeljaka može biti glavni dio regulacije aktivnosti enzima. Interakcija Mg2+ s proteinima također se mora uzeti u obzir za transport iona kroz biološke membrane.[nedostaje referenca]
Mangan
U biološkim sistemima, samo mangan (Mn2+) je lahko sposoban zamijeniti Mg2+, ali samo u ograničenom skupu okolnosti. Mn2+ je vrlo sličan Mg2+ u smislu svojih hemijskih svojstava, uključujući kompleksiranje unutrašnje i vanjske ljuske. Mn2+ efikasno veže ATP i omogućava hidrolizu energetskog molekula većinom ATPaza. Mn2+ također može zamijeniti Mg2+ kao aktivirajući ion za brojne Mg2+-ovisne enzime, iako se obično gubi dio enzimske aktivnosti.[55] Ponekad se takve preferencije enzima prema metalima razlikuju među blisko srodnim vrstama: naprimjer, enzim reverzna transkriptaza lentivirusa poput HIV, SIV i FIV obično ovisi o Mg2+, dok analogni enzim za druge retroviruse preferira Mn2+.
Remove ads
Mjerenje magnezija u biološkim uzorcima
Radioaktivnim izotopima
Upotreba radioaktivnih elemenata za praćenje u testovima unosa iona omogućava izračunavanje km, Ki i Vmax i određuje početnu promjenu u sadržaju iona u ćelijama. **28Mg** se raspada emisijom visokoenergetske beta ili gama čestice, što se može mjeriti pomoću scintilacionog brojača. Međutim, radioaktivni poluživot **28Mg**, najstabilnijeg od radioaktivnih izotopa magnezija, je samo 21 sat. Ovo ozbiljno ograničava eksperimente koji uključuju ovaj nuklid. Također, od 1990. godine nijedan pogon nije rutinski proizvodio **28Mg**, a cijena po mCi se sada predviđa na približno 30.000 američkih dolara.[64] Hemijska priroda Mg2+ je takva da joj se može pribliziti nekoliko drugih kationa.[65] Međutim, Co2+, Mn2+ i Ni2+ su uspješno korišteni za imitiranje svojstava Mg2+ u nekim enzimskim reakcijama, a radioaktivni oblici ovih elemenata su uspješno korišteni u studijama transporta kationa. Teškoća korištenja zamjene metalnih iona u proučavanju funkcije enzima je u tome što je odnos između aktivnosti enzima sa zamjenskim ionom u poređenju sa originalom vrlo teško utvrditi.[65]
Pomoću fluorescentnih indikatora
Brojni helatori dvovalentnih kationa imaju različite fluorescentne spektre u vezanom i nevezanom stanju.[66] Helatori za Ca2+ su dobro utvrđeni, imaju visok afinitet za kation i nisku interferenciju od drugih iona. Mg2+ helatori zaostaju, a glavna fluorescentna boja za Mg2+ (mag-fura 2[67]) zapravo ima veći afinitet za Ca2+.[68] Ovo ograničava primjenu ove boje na tipove ćelija gdje je nivo mirovanja Ca2+ <1 μM i ne varira u zavisnosti od eksperimentalnih uslova pod kojima se Mg2+ mjeri. Nedavno su Otten et al. (2001) opisali rad na novoj klasi spojeva koji bi se mogli pokazati korisnijim, imajući značajno bolji afinitet vezivanja za Mg2+.[69] Upotreba fluorescentnih boja ograničena je na mjerenje slobodnog Mg2+. Ako ćelija puferuje koncentraciju iona helacijom ili uklanjanjem u subćelijske odjeljke, izmjerena brzina apsorpcije će dati samo minimalne vrijednosti km i Vmax.
Po elektrofiziologiji
Prvo, ionski specifične mikroelektrode mogu se koristiti za mjerenje unutrašnje koncentracije slobodnih iona u ćelijama i organelama. Glavne prednosti su što se očitavanja mogu vršiti iz ćelija tokom relativno dugih vremenskih perioda i što se, za razliku od boja, ćelijama dodaje vrlo malo dodatnog kapaciteta puferovanja iona.[70]
Drugo, tehnika dvoelektrodnog naponskog stezanja omogućava direktno mjerenje fluksa iona kroz ćelijsku membranu.[71] Membrana se drži na električnom potencijalu i mjeri se odgovarajuća struja. Svi ioni koji prolaze kroz membranu doprinose izmjerenoj struji.
Treće, tehnika patch-clamp-a koristi izolirane dijelove prirodne ili umjetne membrane na gotovo isti način kao i naponski stezač, ali bez sekundarnih efekata ćelijskog sistema. Pod idealnim uslovima, provodljivost pojedinačnih kanala može se kvantificirati. Ova metodologija daje najdirektnije mjerenje djelovanja ionskih kanala.[71]
Apsorpcijskom spektroskopijom
Plamena atomska apsorpcijska spektroskopija (AAS) određuje ukupni sadržaj magnezija u biološkom uzorku. Ovaj metod je destruktivna; Biološki uzorci moraju se razgraditi u koncentrovanim kiselinama kako bi se izbjeglo začepljenje finog raspršivača. Osim toga, jedino ograničenje je da uzorci moraju biti u zapremini od približno 2 mL i u rasponu koncentracije od 0,1 – 0,4 μmol/L za optimalnu tačnost. Budući da ova tehnika ne može razlikovati Mg2+ koji je već prisutan u ćeliji od onog koji je apsorbovan tokom eksperimenta, može se kvantificirati samo sadržaj koji nije apsorbovan.
Induktivno spregnuta plazma (ICP) korištenjem modifikacija masene spektrometrije (MS) ili atomske emisione spektroskopije (AES) također omogućava određivanje ukupnog sadržaja iona u biološkim uzorcima.[72]
Remove ads
Transport magnezija
Hemijska i biohemijska svojstva Mg2+ predstavljaju značajan izazov za ćelijski sistem prilikom transporta iona kroz biološke membrane. Dogma transporta iona kaže da transporter prepoznaje ion, a zatim progresivno uklanja vodu hidratacije, uklanjajući većinu ili svu vodu na selektivnoj porama prije nego što oslobodi ion na drugoj strani membrane.[73] Zbog svojstava Mg2+, velike promjene volumena od hidratiziranog do golog iona, visoke energije hidratacije i vrlo niske brzine izmjene liganda u unutrašnjoj koordinacijskoj sferi, ovi koraci su vjerovatno teži nego za većinu drugih iona. Do danas je pokazano da je samo ZntA protein Parameciuma Mg2+ kanal.[74] Mehanizmi transporta Mg2+ preostalim proteinima počinju se otkrivati, a prva trodimenzijska struktura transportnog kompleksa Mg2+ je riješena 2004.[75] Hidratacijska ljuska Mg2+ iona ima vrlo čvrsto vezanu unutrašnju ljusku od šest molekula vode i relativno čvrsto vezanu drugu ljusku koja sadrži 12-14 molekula vode (Markham et al., 2002). Stoga se pretpostavlja da prepoznavanje Mg2+ iona zahtijeva neki mehanizam za početnu interakciju s hidratacijskom ljuskom Mg2+, nakon čega slijedi direktno prepoznavanje/vezivanje iona za protein.[64]
Uprkos mehanističkoj teškoći, Mg2+ se mora transportovati kroz membrane, a opisan je veliki broj fluksa Mg2+ kroz membrane iz različitih sistema.[76] Međutim, samo je mali broj Mg2+ transportera okarakteriziran na molekulskom nivou.
Blokada kanala ligandnih iona
Magnezijevi ioni (Mg2+) u ćelijskoj biologiji su obično u gotovo svim smislovima suprotni Ca2+ ionima, jer su i oni bivalentni, ali imaju veću elektronegativnost i stoga vrše veću privlačnost na molekule vode, sprječavajući prolaz kroz kanal (iako je sam magnezij manji). Dakle, Mg2+ ioni blokiraju Ca2+ kanale kao što su (NMDA kanali) i pokazalo se da utiču na kanale gap veza, formirajući električne sinapse.
Remove ads
Fiziologija magnezija u biljkama
Prethodni odjeljci su detaljno obradili hemijske i biohemijske aspekte Mg2+ i njegov transport kroz ćelijske membrane. Ovaj odjeljak će primijeniti ovo znanje na aspekte fiziologije cijele biljke, u pokušaju da pokaže kako ovi procesi interaguju sa većim i složenijim okruženjem višećelijskog organizma.
Nutritivne potrebe i interakcije
Mg2+ je neophodan za rast biljaka i prisutan je u višim biljkama u količinama reda veličine 80'μmol'g−1 suhe težine.[4] Količine Mg2+ variraju u različitim dijelovima biljke i zavise od nutritivnog statusa. U periodima obilja, višak Mg2+ može se skladištiti u vaskularnim ćelijama (Stelzer et al., 1990;[39]), a u periodima gladi Mg2+ se u mnogim biljkama preraspodjeljuje od starijih ka novijim listovima.[4][77]
Mg2+ se apsorbira u biljke putem korijena. Interakcije s drugim kationima u rizosferi mogu imati značajan uticaj na unos iona. (Kurvits i Kirkby, 1980;[78] Struktura ćelijskih zidova korijena je visoko propusna za vodu i ione, te stoga unos iona u ćelije korijena može da se dogodi bilo gdje, od korijenovih dlačica do ćelija koje se nalaze gotovo u centru korijena (ograničeno samo Casparovom trakom). Ćelijski zidovi i membrane biljaka nose veliki broj negativnih naboja, a interakcije kationa s tim nabojima su ključne za unos kationa od strane ćelija korijena, omogućavajući lokalni efekat koncentriranja.[79] Mg2+ se relativno slabo veže za ove naboje i može biti istisnut drugim kationima, što ometa unos i uzrokuje nedostatak u biljci. Unutar pojedinačnih biljnih ćelija, potrebe za Mg2+ su uglavnom iste kao i za sav ćelijski život; Mg2+ se koristi za stabilizaciju membrana, vitalan je za iskorištavanje ATP-a, u velikoj mjeri je uključen u biohemiju nukleinskih kiselina i kofaktor je za mnoge enzime (uključujući ribosom). Također, Mg2+ je koordinirajući ion u molekuli hlorofila. Unutarćelijska kompartmentalizacija Mg2+ u biljnim ćelijama dovodi do dodatne složenosti. Četiri kompartmenta unutar biljne ćelije su prijavila interakcije sa Mg2+. U početku, Mg2+ će ući u ćeliju u citoplazmu (putem još uvijek neidentificiranog sistema), ali koncentracije slobodnog Mg2+ u ovom odjeljku su strogo regulirane na relativno niskim nivoima (≈2 mmol/L) i tako se svaki višak Mg2+ ili brzo izvozi ili skladišti u drugom unutarćelijskom odjeljku, vakuoli.[80] Potreba za Mg2+ u mitohondrijama je dokazana kod kvasca[81] i čini se vrlo vjerovatnim da će se isto odnositi i na biljke. Hloroplasti također zahtijevaju značajne količine internog Mg2+ i niske koncentracije citoplazmatskog Mg2+.[82][83] Osim toga, čini se vjerovatnim da i druge subcelularne organele (npr. Golgijev aparat, endoplazmatski retikulum itd.) također zahtijevaju Mg2+.
Distribucija magnezijevih iona unutar biljke
Jednom kada se nađe u citoplazmatskom prostoru korijenskih ćelija, Mg2+, zajedno s drugim kationima, vjerovatno se radijalno transportuje u stelu i vaskularno tkivo.[84] Iz ćelija koje okružuju ksilem, ioni se oslobađaju ili pumpaju u ksilem i prenose kroz biljku. U slučaju Mg2+, koji je vrlo mobilan i u ksilemu i u floemu,[85] Ioni će biti transportovani do vrha biljke i nazad u kontinuiranom ciklusu obnavljanja. Stoga je unos i oslobađanje iz vaskularnih ćelija vjerovatno ključni dio homeostaze Mg2+ cijele biljke. Slika 1 pokazuje koliko je malo procesa povezano s njihovim molekulskim mehanizmima (samo je vakuolski unos povezan s transportnim proteinom, AtMHX).
Dijagram prikazuje shematski prikaz biljke i pretpostavljene procese transporta Mg2+ u korijenu i listu gdje se Mg2+ učitava i istovaruje iz vaskularnih tkiva.[4] Mg2+ se unosi u prostor ćelijskog zida korijena (1) i interaguje s negativnim nabojima povezanim sa ćelijskim zidovima i membranama. Mg2+ se može odmah apsorbirati u ćelije (simplastični put) ili može putovati sve do Casparijeve trake (4) prije nego što se apsorbira u ćelije (apoplastični put; 2). Koncentracija Mg2+ u ćelijama korijena vjerovatno je puferirana skladištenjem u vakuolama korijenskih ćelija (3). Treba napomenuti da ćelije u vrhu korijena ne sadrže vakuole. Jednom kada se nađe u citoplazmi korijenskih ćelija, Mg2+ putuje prema centru korijena putem plazmodezmi, gdje se unosi u ksilem (5) radi transporta do gornjih dijelova biljke. Kada Mg2+ stigne do listova, istovaruje se iz ksilema u ćelije (6) i ponovo se puferira u vakuolama (7). Nije poznato da li se kruženje Mg2+ u floem odvija putem općih ćelija u listu (8) ili direktno iz ksilema u floem putem zvanim transfer ćelija (9). Mg2+ se može vratiti u korijenje u floemskom soku.

Kada ćelija apsorbuje Mg2+ ion kojem je potreban za metaboličke procese, generalno se pretpostavlja da ion ostaje u toj ćeliji sve dok je ćelija aktivna.[4] U vaskularnim ćelijama to nije uvijek slučaj; u periodima obilja, Mg2+ se skladišti u vakuoli, ne učestvuje u svakodnevnim metaboličkim procesima ćelije (Stelzer et al., 1990) i oslobađa se po potrebi. Ali za većinu ćelija, smrt starenjem ili povredom oslobađa Mg2+ i mnoge druge ionske sastojke, reciklirajući ih u zdrave dijelove biljke. Osim toga, kada je Mg2+ u okolini ograničavajući, neke vrste su u stanju mobilizirati Mg2+ iz starijih tkiva.[77] Ovi procesi uključuju oslobađanje Mg2+ iz vezanog i uskladištenog stanja i njegov transport nazad u vaskularno tkivo, gdje se može distribuirati u ostatak biljke. U periodima rasta i razvoja, Mg2+ se također remobilizira unutar biljke kako se mijenjaju odnosi izvora i ponora.[4]
Homeostaza Mg2+ unutar pojedinačnih biljnih ćelija održava se procesima koji se odvijaju na plazma membrani i na membrani vakuole (vidi Sliku 2). Glavna pokretačka sila za translokaciju iona u biljnim ćelijama je ΔpH.[86] H+-ATPaze pumpaju H+ ione protiv svog gradijenta koncentracije kako bi održale pH diferencijal koji se može koristiti za transport drugih iona i molekula. H+ ioni se pumpaju iz citoplazme u ekstracelularni prostor ili u vakuolu. Ulazak Mg2+ u ćelije može se dogoditi kroz jedan od dva puta, putem kanala koristeći ΔΨ (negativna unutrašnja strana) preko ove membrane ili putem simport sa H+ ionima. Za transport Mg2+ iona u vakuolu potreban je Mg2+/H+ antiport transporter (kao što je AtMHX). H+-ATPaze zavise od Mg2+ (vezanog za ATP) za aktivnost, tako da je Mg2+ potreban za održavanje vlastite homeostaze.
Prikazan je shematski prikaz biljne ćelije, uključujući četiri glavna odjeljka za koja se trenutno zna da interaguju sa Mg2+. H+-ATPaze održavaju konstantnu ΔpH kroz plazma membranu i membranu vakuole. Mg2+ se transportuje u vakuolu koristeći energiju ΔpH (kod A. thaliana pomoću AtMHX). Transport Mg2+ u ćelije može koristiti ili negativni ΔΨ ili ΔpH. Transport Mg2+ u mitohondrije vjerovatno koristi ΔΨ kao u mitohondrijama kvasca, i vjerovatno je da hloroplasti preuzimaju Mg2+ sličnim sistemom. Mehanizam i molekularna osnova za oslobađanje Mg2+ iz vakuola i iz ćelije nisu poznati. Slično tome, promjene koncentracije Mg2+ u hloroplastima regulisane svjetlošću nisu u potpunosti razjašnjene, ali zahtijevaju transport H+ iona preko tilakoidne membrane.

Magnezij, hloroplasti i fotosinteza
Mg2+ je koordinirajući metalni ion u molekulu hlorofila, a u biljkama gdje je ion u velikoj količini oko 6% ukupnog Mg2+ je vezano za hlorofil.[4][87][88] Slaganje tilakoida stabilizirano je pomoću Mg2+ i važno je za efikasnost fotosinteze, omogućavajući fazne prijelaze.[89]
Mg2+ se vjerovatno u najvećoj mjeri apsorbira u hloroplaste tokom razvoja izazvanog svjetlošću od proplastida do hloroplasta ili etioplasta do hloroplasta. U tim trenucima, sinteza hlorofila i biogeneze tilakoidnih membranskih slojeva apsolutno zahtijevaju dvovalentni kation.[90][91] Da li se Mg2+ može kretati u i izvan hloroplasta nakon ove početne razvojne faze bilo je predmet nekoliko kontradiktornih izvještaja. Deshaies et al. (1984) su otkrili da se Mg2+ kretao u i izvan izoliranih hloroplasta iz mladih biljaka graška,[92] ali Gupta i Berkowitz (1989) nisu uspjeli reproducirati rezultat koristeći starije hloroplaste špinata.[93] Deshaies i saradnici su u svom radu naveli da stariji hloroplasti graška pokazuju manje značajne promjene u sadržaju Mg2+ od onih koji su korišteni za formiranje njihovih zaključaka. Relativni udio nezrelih hloroplasta prisutnih u preparatima može objasniti ova zapažanja. Metaboličko stanje hloroplasta znatno se mijenja između noći i dana. Tokom dana, hloroplast aktivno sakuplja energiju svjetlosti i pretvara je u hemijsku energiju. Aktivacija uključenih metaboličkih puteva dolazi od promjena u hemijskoj prirodi strome pri dodavanju svjetlosti. H+ se ispumpava iz strome (i u citoplazmu i u lumen) što dovodi do alkalnog pH.[94][95] Mg2+ (zajedno sa K+) se oslobađa iz lumena u stromu, u procesu elektroneutralizacije, kako bi se uravnotežio protok H +.[96][97][98][99] Konačno, tiolne grupe na enzimima se redukuju promjenom redoks stanja strome.[100] Primjeri enzima aktiviranih kao odgovor na ove promjene su fruktoza 1,6-bisfosfataza, sedoheptuloza bisfosfataza i ribuloza-1,5-bisfosfat karboksilaza.[4][58][100] Tokom tamnog perioda, ako bi ovi enzimi bili aktivni, došlo bi do rasipnog kruženja produkata i supstrata.
Mogu se identificirati dvije glavne klase enzima koji interaguju sa Mg2+ u stromi tokom svjetlosne faze.[58] Prvo, enzimi u glikolitičkom putu najčešće interaguju sa dva atoma Mg2+. Prvi atom djeluje kao alosterički modulator aktivnosti enzima, dok drugi formira dio aktivnog mjesta i direktno je uključen u katalitičku reakciju. Druga klasa enzima uključuje one gdje je Mg2+ kompleksiran sa nukleotidnim di- i trifosfatima (ADP i ATP), a hemijska promjena uključuje prijenos fosforila. Mg2+ može također imati ulogu u strukturnom održavanju ovih enzima (npr. enolaza).
Stres uzrokovan magnezijem
Reakcije biljaka na stres mogu se primijetiti kod biljaka koje su nedovoljno ili previše opskrbljene Mg2+. Prvi uočljivi znakovi stresa uzrokovanog Mg2+ kod biljaka, kako zbog gladovanja tako i zbog toksičnosti, je smanjenje brzine fotosinteze, što se pretpostavlja zbog jakih veza između Mg2+ i hloroplasta/hlorofila. Kod borova, čak i prije vidljive pojave žutih i nekrotičnih mrlja, fotosintetska efikasnost iglica značajno opada.sinteze proteina[77] Kod nedostatka Mg2+, prijavljeni sekundarni efekti uključuju nepokretljivost ugljikohidrata, gubitak transkripcije RNK i gubitak sinteze proteina. Međutim, zbog pokretljivosti Mg2+ unutar biljke, fenotip nedostatka može biti prisutan samo u starijim dijelovima biljke. Naprimjer, kod Pinus radiata kojem nedostaje Mg2+, jedan od najranijih znakova identifikacije je hloroza u iglicama na donjim granama drveta. To je zato što je Mg2+ oporavljen iz ovih tkiva i premješten u rastuće (zelene) iglice više na drvetu.[77]
Deficit Mg2+ može biti uzrokovan nedostatkom iona u mediju (tlu), ali češće dolazi od inhibicije njegovog usvajanja.[4] Mg2+ se prilično slabo veže za negativno nabijene grupe u ćelijskim zidovima korijena, tako da višak drugih kationa kao što su K+, NH4+, Ca2+ i Mn2+ može ometati usvajanje. U kiselim zemljištima Al3+ je posebno jak inhibitor apsorpcije Mg2+.[101][102] Inhibicija preko Al3+ i Mn2+ je ozbiljnija nego što se može objasniti jednostavnim istiskivanjem, stoga je moguće da se ovi ioni direktno vežu za sistem unosa Mg2+.[4] Kod bakterija i kvasaca, takvo vezivanje putem Mn2+ je već uočeno. Stresne reakcije u biljci se razvijaju kada se ćelijski procesi zaustavljaju zbog nedostatka Mg2+ (npr. održavanje ΔpH kroz plazma i vakuolske membrane). Kod biljaka kojima nedostaje Mg2+ u uslovima slabog osvjetljenja, procenat Mg2+ vezanog za hlorofil zabilježen je na 50%.[103] Vjerovatno je da ova neravnoteža ima štetne učinke na druge ćelijske procese.
Stres uzrokovan toksičnošću Mg2+ je teže razviti. Kada je Mg2+ obilan, biljke uglavnom uzimaju ion i skladište ga (Stelzer et al., 1990). Međutim, ako nakon toga slijedi suša, tada se koncentracije iona unutar ćelije mogu dramatično povećati. Visoke citoplazmatske koncentracije Mg2+ blokiraju K+ kanal u unutrašnjoj membrani omotača hloroplasta, što zauzvrat inhibira uklanjanje H+ iona iz strome hloroplasta. To dovodi do zakiseljavanja strome koja inaktivira ključne enzime u fiksaciji ugljika, što sve dovodi do proizvodnje slobodnih radikala kisika u hloroplastu koji zatim uzrokuju oksidativna oštećenja.[104]
Remove ads
Također pogledajte
- Biologija i farmakologija hemijskih elemenata
- Kalcij u biologiji
- Jod u biologiji
- Ionski kanali
- Nedostatak magnezija (poljoprivreda)
- Nedostatak magnezija
- Mayersov koktel
- Osteoporoza
- Kalij u biologiji
- Selen u biologiji
- Natrij u biologiji
Napomene
Reference
Vanjski linkovi
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads
