tipo de hormonas esteroides From Wikipedia, the free encyclopedia
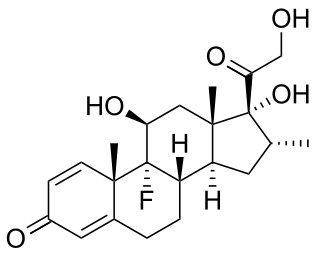
Os glicocorticoides (GCs) son unha clase de corticosteroides, un tipo de hormonas esteroides entre as que a máis salientable é o cortisol. Un sinónimo menos común que se utiliza ás veces para eles é glicocorticosteroide. Os glicocorticoides son corticosteroides que se unen ao receptor de glicocorticoides,[1] o cal está presente practicamente en todas as células de vertebrados. O nome glicocorticoide (de glicosa + córtex + esteroide) deriva do seu papel na regulación do metabolismo da glicosa, a súa síntese no córtex adrenal, e a súa estrutura química de esteroide (ver estrutura na imaxe á dereita).

Os glicocorticoides forman parte do mecanismo de retroalimentación do sistema inmunitario, que reduce certos aspectos da función inmunitaria, como a redución da inflamación. Por esa razón, utilízanse tamén en medicina para tratar doenzas causadas por un sistema inmunitario sobreactivado, como as alerxias, asma, enfermidades autoinmunes, e sepse. Os glicocorticoides teñen moitos e diversos efectos (pleiotrópicos), entre eles algúns efectos secundarios potencialmente nocivos, e como resultado adoitan venderse só con receita médica.[2] Tamén interfiren con algúns dos mecanismos anormais que presentan as células cancerosas, polo que se usan en altas doses para tratar certos cancros. Isto inclúe principalmente efectos inhibidores sobre a proliferación de linfocitos (tratamento de linfomas e leucemias) e a mitigación dos efectos secundarios dos fármacos anticancro.
Os glicocorticoides causan os seus efectos uníndose ao receptor de glicocorticoides. O complexo do receptor de glicocorticoides activado, á súa vez, regula á alza a expresión de proteínas antiinflamatorias no núcleo celular (un proceso chamado transactivación) e reprime a expresión de proteínas proinflamatorias no citosol ao impedir a translocación doutros factores de transcrición do citosol ao núcleo (transrepresión).[2]
Os glicocorticoides distínguense dos mineralocorticoides e dos esteroides sexuais polos seus receptores específicos, células diana, e efectos. En termos técnicos, "corticosteroide" refírese tanto aos glicocorticoides coma aos mineralocorticoides (xa que ambos os dous son hormonas similares producidas polo córtex adrenal), aínda que ás veces se usa como sinónimo de "glicocorticoide". Os glicocorticoides prodúcense principalmente na zona fasciculada do córtex adrenal, mentres que os mineralocorticoides sintetízanse na zona glomerulosa.
O cortisol (ou hidrocortisona) é o glicocorticoide humano máis importante. É esencial para a vida, e regula ou mantén unha variedade de importantes funcións cardiovasculares, metabólicas, inmunolóxicas, e homeostáticas. Disponse ademais de varios glicocorticoides sintéticos, que se usan como terapia de substitución nas deficiencias de glicocorticoides ou para suprimir o sistema inmunitario.

Os efectos dos glicocorticoides poden ser grosso modo clasificados en dúas grandes categorías: inmunolóxicos e metabólicos. Ademais, os glicocorticoides xogan un importante papel no desenvolvemento fetal e na homeostase dos fluídos corporais.
Como se discute con máis detalle máis adiante, os glicocorticoides funcionan por medio da interacción co receptor de glicocorticoides orixinando:
Os glicocorticoides tamén desempeñan un papel no desenvolvemento e homeostase dos linfocitos T. Isto observouse en ratos transxénicos que tiñan a sensibilidade da liñaxe de células T para os glicocorticoides incrementada ou diminuída.[3]
O nome "glicocorticoide" deriva das observacións iniciais de que estas hormonas estaban implicadas no metabolismo da glicosa. En estado de xexún, o cortisol estimula varios procesos que serven en conxunto para incrementar e manter as concentracións normais de glicosa no sangue.
Efectos metabólicos:
Os niveis excesivos de glicocorticoides orixinados pola administración de fármacos ou polo hiperadrenocorticismo teñen efectos en moitos sistemas. Algúns exemplos son a inhibición da formación do óso, a supresión da absorción do calcio (ambas as cousas poden orixinar osteoporose), retardo da curación de feridas, debilidade muscular, e un incremento do risco de infección. Estas observacións suxiren que os glicocorticoides exercen outra multitude de funcións fisiolóxicas menos relevantes.[3]
Os glicocorticoides teñen múltiples efectos sobre o desenvolvemento fetal. Un importante exemplo é o seu papel na promoción da maduración do pulmón e a produción do surfactante pulmonar necesario para a función pulmonar extrauterina. Os ratos con alteracións homocigotas no xene da hormona liberadora da corticotropina (véxase máis abaixo) morren ao nacer debido á súa inmadureza pulmonar. Ademais, os glicocorticoides son necesarios para o desenvolvemento normal do cerebro, ao iniciaren a maduración terminal, remodelaren os axóns e dendritas, e afectaren á supervivencia celular,[4] e poden xogar tamén un papel no desenvolvemento do hipocampo.

Os glicocorticoides actúan sobre o hipocampo, amígdala, e lobos frontais. Xunto coa adrenalina, favorecen a formación de memorias flash de aconecementos asociados con fortes emocións, tanto positivas coma negativas.[5] Isto foi confirmado en varios estudos, nos que o bloqueo da actividade dos glicocorticoides ou da noradrenalina diminuía a lembranza de información emocionalmente relevante. Fontes adicionais atoparon que suxeitos cuxa memoria de episodios de medo estaba acompañada por altos niveis de cortisol tiñan unha mellor consolidación desta memoria (este efecto era máis importante en homes). O efecto que teñen os glicocorticoides sobre a memoria pode deberse a danos que afectan especificamente á área CA1 do hipocampo. En moitos estudos en animais, o estrés prolongado (que causa un incremento prolongado dos niveis de glicocorticoides) causaba a destrución de neuronas nesa área do cerebro, a cal foi conectada co desempeño da memoria.[6][7][8]
Os glicocorticoides teñen tamén un significativo impacto sobre a vixilancia (trastorno de déficit de atención) e a cognición (memoria). Isto parece seguir a curva de Yerkes-Dodson, xa que se detectou que na gráfica os "niveis circulantes de glicocorticoides" fronte a "desempeño da memoria" seguían un patrón de U invertido, moi similar á curva de Yerkes-Dodson. Por exemplo, a potenciación a longo prazo (o proceso de formación de recordos a longo prazo) é óptima cando os niveis de glicocorticoides están lixeiramente elevados, mentres que hai unha diminución significativa desta potenciación despois dunha adrenalectomía (estado baixo en glicocorticoides) ou despois da administración exóxena de glicocorticoides (estado de alto nivel de glicocorticoides). Os niveis elevados de glicocorticoides potencian a memoria de acontecementos que excitan as emocións, pero levan máis a miúdo a unha mala memoria de material non relacionado coa fonte da excitación emocional/estrés.[9] A diferenza dos efectos de potenciación dependentes da dose dos glicocorticoides sobre a cosolidación da memoria, estas hormonas do estrés inhiben a recuperación de información xa almacenada.[10] A exposición a longo prazo a medicacións con glicocorticoides, como as medicacións contra o asma e antiinflamatorias xera déficits de memoria e atención tanto durante coma, en menor medida, despois do tratamento,[11][12] unha condición coñecida como "demencia de esteroides."[13]
Os glicocorticoides poderían actuar centralmente, e tamén perifericamente, para axudar na normalización do volume de fluído extracelular ao regular a acción do péptido natriurético auricular (ANP), actuando centralmente (no hipotálamo) e perifericamente (nos riles).[14][15]
Un tratamento prolongado con glicocorticoides fai decrecer a densidade de receptores CB1 de cannabinoides CB1 no hipocampo.[16]
Os glicocorticoides únense ao receptor de glicocorticoides citosólico, un tipo de receptor nuclear que é activado pola unión dun ligando. Unha vez que unha hormona se une ao correspondente receptor, o complexo acabado de formar translócase ao núcleo celular, onde se une aos elementos de resposta aos glicocorticoides (GRE) situados na rexión promotora dos xenes diana, o que ten como resultado a regulación da expresión xénica. Este proceso denomínase xeralmente activación transcricional ou transactivación.[17][18]
As proteínas codificadas por estes xenes regulados á alza teñen unha gran variedade de efectos, incluíndo, por exemplo:[18]
O mecanismo oposto denomínase represión transcricional ou transrepresión. A idea clásica sobre o funcionamento deste mecanismo é que o receptor de glicocorticoideds activado se une ao ADN no mesmo sitio onde se uniría outro factor de transcrición, o cal impide a transcrición de xenes que se transcriben grazas á actividade dese factor.[17][18] Aínda que esta interferencia ocorre, os resultados non son consistentes para todos os tipos celulares e condicións, e non hai ningún mecanismo xeral aceptado comunmente para explicar esta transrepresión.[18]
Estanse a descubrir novos mecanismos nos que a transcrición é reprimida, pero o receptor de glicocorticoides activado non interacciona co ADN, senón que interacciona directamente con outro factor de transcrición, interferindo con el, ou interacciona con outras proteínas que interfiren á súa vez coa función doutros factores de transcrición. Este último mecanismo parece ser o modo máis probable no que o receptor de glicoproteínas activado interfire co NF-κB, concretamente recrutando a histona deacetilase, a cal desacetila o ADN na rexión do promotor, o que produce o peche da estrutura da cromatina no lugar onde o NF-κB ten que unirse.[17][18]
O receptor de glicocorticoides activado ten efectos que se demostrou experimentalmente que eran independentes de calquera efecto sobre a súa transcrición e só poden deberse á unión directa do receptor de glicocorticoides activado con outras proteínas ou co ARNm.[17][18]
Por exemplo, a Src quinase que se une ao receptor de glicocorticoides inactivo, libérase cando un glicocorticoide se une ao receptor de glicocorticoides, e fosforila unha proteína que á súa vez despraza do receptor unha proteína adaptadora, que é importante na inflamación e que é o factor de crecemento epidérmico (EGF), reducindo a súa actividade, o cal á súa vez ten como resultado a redución da formación de ácido araquidónico, unha molécula proinflamatoria clave. Este é un mecanismo polo cal os glicocorticoides teñen un efecto antiinflamatorio.[17]
Para usos terapéuticos creáronse diversos glicocorticoides sintéticos, algúns moito máis potentes que o cortisol. Diferéncianse tanto na farmacocinética (factor de absorción, vida media, volume de distribución, aclaramento) coma na farmacodinámica (por exemplo a capacidade de actividade de mineralocorticoide: retención de sodio (Na+) e auga; fisioloxía renal). Como poden permear o intestino doadamente, adminístranse principalmente por vía oral, pero tamén por outros métodos, como de forma tópica sobre a pel. Máis do 90% deles únense a diferentes proteínas plasmáticas, aínda que cunha diferente especificiadde de unión. Os glicocorticoides endóxenos e algúns corticoides sintéticos teñen alta afinidade coa proteína transcortina (tamén chamada glubulina ligadora de corticosteroides), mentres que todos eles se unen á albumina sérica. No fígado, metabolízanse rapidamente por conxugación cun sulfato ou ácido glicurónico, e son segregados á urina.
A potencia, duración dos efectos e a potencia de mineralocorticoide solapada dos glicocorticoides varía. O cortisol (hidrocortisona) é o estándar para a comparación para a potencia de glicocorticoides. A hidrocortisona é o nome que se usa para as preparacións farmacéuticas do cortisol.
Os datos da táboa refírense a doses orais, excepto cando se indica outra cousa. A potencia oral pode ser menor que a parenteral porque cantidades significativas (de ata o 50% nalgúns casos) pode non ser absorbido no intestino. A fludrocortisona, DOCA (Desoxicorticosterona acetato), e a aldosterona non son, por definición, considerados glicocorticoides, aínda que poden ter unha potencia menor de glicocorticoide, e incluíronse nesta táboa para proporcionar perspectiva sobre a potencia de mineralocorticoide.
| Nome | Potencia de glicocorticoide | Potencia de mineralocorticoide | Duración da acción (t1/2 en horas) |
|---|---|---|---|
| Cortisol (hidrocortisona) | 1 | 1 | 8 |
| Cortisona | 0,8 | 0,8 | oral 8, intramuscular 18+ |
| Prednisona | 3,5-5 | 0,8 | 16-36 |
| Prednisolona | 4 | 0,8 | 16-36 |
| Metilprednisolona | 5-7,5 | 0,5 | 18-40 |
| Dexametasona | 25-80 | 0 | 36-54 |
| Betametasona | 25-30 | 0 | 36-54 |
| Triamcinolona | 5 | 0 | 12-36 |
| Beclometasona | - | - | - |
| Fludrocortisona acetato (non glicocorticoide) | 15 | 200 | 24 |
| Desoxicorticosterona acetato (DOCA) (non glicocorticoide) | 0 | 20 | - |
| Aldosterona (non glicocorticoide) | 0,3 | 200-1000 | - |
Os glicocorticoides poden usarse en baixas doses na insuficiencia adrenal. A doses moito máis altas, os glicocorticoides orais ou inhalados son utilizados para suprimir varios trastornos inflamatorios, alérxicos, e autoinmunes. Os glicocorticoides inhalados son o tratamento de segunda liña para o asma. Tamén se administran como inmunosupresores postransplante para impedir o rexeitamento de transplantes agudo e a enfermidade de enxerto contra hóspede. Non obstante, non impiden unha infección e ademais inhiben o posterior proceso reparativo. Novas evidencias indican que os glicocorticoides poderían utilizarse no tratamento da insuficiencia cardíaca para incrementar a resposta renal aos péptidos diuréticos e natreiuréticos.
Todos os glicocorticoides poden administrarse nunha dose que proporciona aproxiadamente o mesmo efecto de glicocorticoide que a produción normal de cortisol; isto refírese a unha dose fisiolóxica, de substtución, ou de mantemento. Esta é de aproximadamente de 6–12 mg/m²/día de hidrocortisona (m² refírese aquí á área superficial corporal, e é unha medida do tamaño do corpo; esta área nun home medio é de 1,9 m²).
Ver a sección sobre "Inmunodeficiencia" máis abaixo para os efectos adversos.
Os glicocorticoides causan inmunosupresión, e o compoñente terapéutico deste efecto é principalmente o decrecemento na función e número de linfocitos, incluíndo tanto as células B coma as T.
O principal mecanismo para esta inmunosupresión é por medio da inhibición do factor nuclear amplificador da cadea lixeira kappa de células B activadas (NF-κB). O NF-κB é un factor de transcrición crítico implicado na síntese de moitos mediadores (é dicir, citocinas) e proteínas (é dicir, proteínas de adhesión) que promoven a resposta inmune. A inhibición deste factor de transcrición, por tanto, mitiga a capacidade do sistema inmunitario de realizar unha resposta.[2]
Os glicocorticoides suprimen a inmunidade celular ao inhibiren xenes que codifican as citocinas IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8 e IFN-γ, a máis importante das cales é IL-2. Unha menor produción de citocinas reduce a proliferación de células T.[21]
Porén, os glicocorticoides non só reducen a proliferación de células T, senón que tamén producen outro efecto ben coñecido: a apoptose inducida por glicocorticoides. O efecto é máis acusado en células T inmaturas que aínda están no timo, pero as células T periféricas tamén son afectadas. O mecanismo exacto que regula esta sensibilidade de glicocorticoides depende do xene Bcl-2.[22]
Os glicocorticoides tamén suprimen a inmunidade humoral, o que causa unha deficiencia inmunitaria humoral. Os glicocorticoides causan que as células B expresen cantidades menores de IL-2 e de receptores de IL-2. Isto diminúe tanto a expansión clonal de células B coma a síntese de anticorpos. A diminución da cantidade de IL-2 tamén causa que se activen menos linfocitos T.
O efecto dos glicocorticoides sobre a expresión do receptor Fc en células inmunitarias é complicado. A dexametasona fai decrecer a expresión de Fc gamma RI simulado por IFN-gamma en neutrófilos mentres inversamente causa o seu incremento nos monocitos.[23] Os glicocorticoides poden tamén facer decrecer a expresión de receptores Fc en macrófagos,[24] pero as probas que apoiaban esta regulación en estudos anteriores foron cuestionadas.[25] O efecto da expresión do receptor Fc en macrófagos é importante xa que cómpre para a fagocitose das células opsonizadas. Isto é así porque os receptores Fc se unen a anticorpos unidos a células marcadas para ser destruídas por macrófagos.
Os glicocorticoides son potentes antiinflamatorios, sen importar cal sexa a causa da inflamación. O seu principal mecanismo antiinflamatorio é a síntese de lipocortina-1 (anexina-1). A lipocortina-1 suprme por un lado a fosfolipase A2, o que bloquea a produción de eicosanoides, e por outro inhibe varios eventos inflamatorios dos leucocitos (adhesión epìtelial), emigración, quimiotaxe, fagocitose, explosión respiratoria, etc). Noutras palabras, os glicocorticoides non só suprimen a resposta inmune senón que tamén inhiben os dous principais produtos da inflamación, que son as prostaglandinas e os leucotrienos. Inhiben a síntese de prostaglandinas a nivel da fosfolipase A2 e da ciclooxixenase/PGE isomerase (COX-1 e COX-2);[26] este último efecto é moisimilar ao dos AINEs, potenciando o efecto antiinflamatorio.
Os glicocorticoides comercializados como antiinflamatorios son xeralmente formulacións de uso tópico, como sprais nasais para a rinite ou inhaladores (de dose medida ou de po seco) para a asma. Estas preparacións teñen a vantaxe de que afectan só á zona onde se aplican, reducindo así os efectos laterais ou as interaccións potenciais. Neste caso, os principais compostos usados son a beclometasona, budesonide, fluticasona, mometasona e ciclesonide.[27]
Os glicocorticoides poden utilizarse no mantemento do hiperaldosteronismo familiar de tipo 1, aínda que non son efectivos para o tipo 2.

A resistencia do organismo ao uso terapéutico dos glicocorticoides pode presentar dificultades; por exemplo, o 25% dos casos graves de asma poden non responder aos esteroides. Isto pode ser o resultado da predisposición xenética, exposición a un produto que causa inflamación (como un alérxeno), fenómenos inmunolóxicos que sortean o efecto dos glicocorticoides, e alteracións farmacocinéticas (absorción incompleta ou excreción ou metabolismo acelerados).[21]
Os glicocorticoides poderían usarse no tratamento da insuficiencia cardíaca descompensada para potenciar a sensibilidade renal aos diuréticos, especialmente en pacientes con insuficiencia cardíaca e resistencia diurética refractaria con grandes doses de diuréticos bucle.[28][29][30][31][32][33][34]
Os fármacos glicocorticoides que se usan actualmente actúan de forma non selectiva, polo que a longo prazo poden alterar moitos procesos anabólicos saudables. Para impediren isto, moitas das investigacións actuais están enfocadas a elaborar fármacos glicocorticoides de acción selectiva. Os seus efectos secundarios inclúen:
A altas doses, a hidrocortisona (cortisol) e os glicocorticoides con potencia apreciable de mineralocorticoide poden exercer tamén un efecto de mineralocorticoide, aínda que en doses fisiolóxicas isto é impedido pola rápida degradación do cortisol pola 11β-hidroxiesteroide deshidroxenase isoencima 2 (11β-HSD2) en tecidos diana dos mineralocorticoides. Os efectos de mineralocorticoide poden ser os seguintes: retención de auga e sales, aumento do volume do fluído extracelular, hipertensión, depleción do potasio, e alcalose metabólica.
Os glicocorticoides causan inmunosupresión, diminuíndo a función e/ou o número de neutrófilos, linfocitos (tanto os B coma os T), monocitos, macrófagos, e a funión de barreira anatómica da pel.[38] Esta supresión, se é grande dabondo, pode causar manifestacións de inmunodeficiencia, incluíndo a deficiencia de células T, a deficiencia inmune humoral e a neutropenia.
| Bacterias |
|
|---|---|
| Fungos |
|
| Virus |
|
| Outros |
|
Ademais dos efectos mencionados antes, o uso de altas doses de esteroides durante máis dunha semana empeza a producir unha supresión das glándulas adrenais do paciente, porque os glicocorticoides exóxenos suprimen a hormona liberadora de corticotropina hipotalámica e a hormona adrenocorticotrópica hipofisaria. Cunha supresión prolongada, as glándulas adrenais atrófianse (encollen fisicamente), e pode tardarse meses en recuperar o seu funcionamento pleno despois de cesar a administración de glicocorticoides exóxenos.
Durante este tempo de recuperación, o paciente é vulnerable á insuficiencia adrenal durante os momentos de estrés, como pode ser unha doenza. Aínda que a dose supresiva e o tempo de recuperación adrenal varían amplamente, as directrices clínicas foron pensadas para estimar a potencial supresión e recuperación adrenais, para reducir así o risco para o paciente. Un exemplo é o seguinte:
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.