トップQs
タイムライン
チャット
視点
核小体
ウィキペディアから
Remove ads
核小体(かくしょうたい、英: nucleolus)は、真核細胞の細胞核中に存在する最大の構造体である[1]。仁、核仁とも呼ばれる。リボソーム生合成の場として最もよく知られているが、シグナル認識粒子の形成や、細胞のストレス応答にも関与している[2]。核小体はタンパク質、DNA、RNAから構成され、核小体形成域と呼ばれる特定の染色体領域の周囲に形成される。核小体の機能不全は"nucleolopathy"と呼ばれるいくつかのヒト疾患の原因となり[3][4]、またがん化学療法の治療標的としての研究も行われている[5][6]。

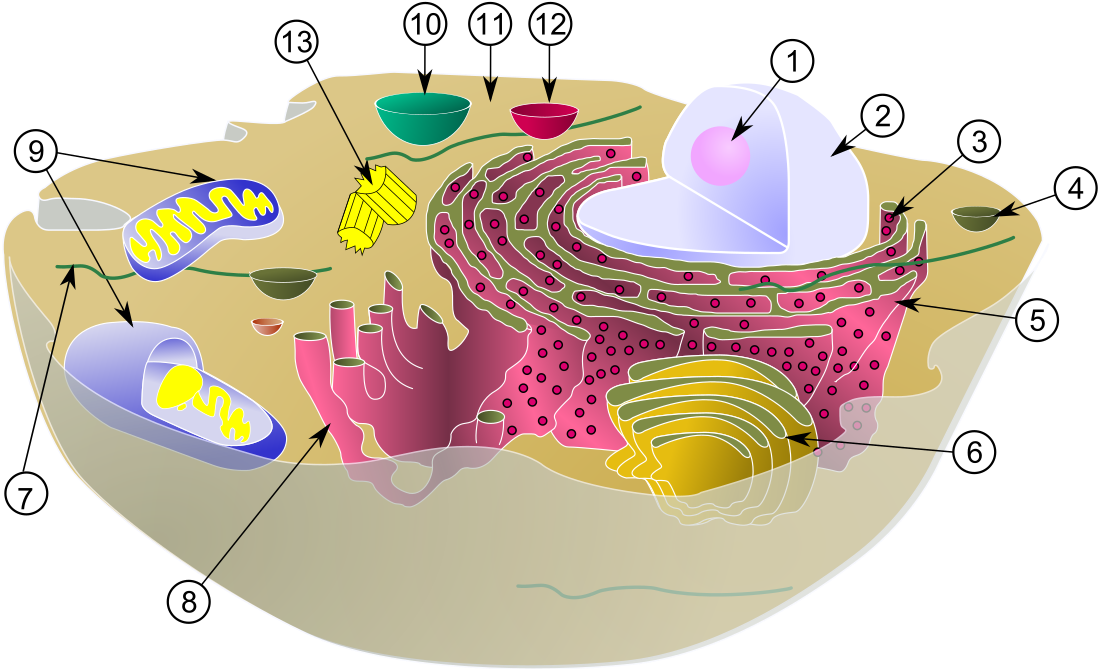
核小体はオレンジ色の球体として示されている
Remove ads
歴史
核小体は1830年代に光学顕微鏡を用いた明視野観察によって同定された[7]。テオドール・シュワンは1839年に発表した論文において、マティアス・ヤーコプ・シュライデンが核内に小体を同定し、その構造体を"Kernkörperchen"と命名していたことを記載している。1847年にこの著作が英語へ翻訳されるにあたって、この構造は"nucleolus"と命名された[8][9]。
その後も核小体の機能に関してはほとんど明らかにされておらず、1964年のジョン・ガードンとドナルド・ブラウンによるアフリカツメガエルXenopus laevisを用いた核小体の研究[10]によって、その機能や詳細な構造に対して多くの関心が寄せられるようになった。彼らはカエル卵の25%には核小体が存在せず、こうした卵では発生が起こらないことを発見した。卵の半数には核小体が1つ、残りの25%には2つ存在しており、彼らは核小体が生命に必要な機能を有すると結論付けた。1966年、Max L. Birnstielらによる核酸ハイブリダイゼーション実験によって、核小体内のDNAがリボソームRNAをコードしているもの(リボソームDNA)であることが示された[11][12]。
Remove ads
構造
核小体には、繊維状中心部(fibrillar center [FC])、高密度繊維状部(dense fibrillar component [DFC])、顆粒部(granular component [GC])という3つの主要な構成要素が知られている[1]。リボソームDNA(rDNA)の転写はFCで行われる[13]。DFCにはフィブリラリンが含まれ[13]、このタンパク質はリボソームRNA(rRNA)のプロセシングに重要である。GCにはヌクレオフォスミンが含まれ[13]、このタンパク質もリボソーム生合成に関与している。
しかしながら、こうした形での組織化は高等真核生物でのみ観察され、無羊膜類から有羊膜類への変化とともに2区画から3区画へと進化したと提唱されている。DNAの遺伝子間領域の大幅な増加を反映して、もともとの繊維状部がFCとDFCへと分離した可能性がある[14]。
多くの核小体(特に植物)の内部に同定されている他の構造として、中心部の透明な領域が核小体空胞(nucleolar vacuole)と呼ばれている[15]。さまざまな植物種の核小体は、ヒトや動物細胞の核小体とは異なり、非常に高濃度の鉄が含まれていることが示されている[16]。
核小体の微細構造は電子顕微鏡によって観察され、その組織化やダイナミクスは蛍光タンパク質標識と光退色後蛍光回復法(FRAP)によって研究されている。免疫蛍光実験においては、PAF49タンパク質が核小体マーカーとして利用される場合がある[17]。
通常、観察される核小体は1つまたは2つであるが、ヒトの二倍体細胞には核小体形成域(NOR)は10個存在するため、より多くの核小体が観察される可能性もある。ほとんどの場合、各核小体には複数のNORが関与している[18]。
Remove ads
機能とリボソームの組み立て
要約
視点

rRNAの転写には、真核生物の3種類のRNAポリメラーゼのうちの2つ(Pol IとPol III)が必要であり、両者は協調的に機能する。第一段階では、rRNAをコードする遺伝子は核小体内でPol Iによって1つの単位として転写される。この転写が起こるためには、いくつかのPol I結合因子とDNA特異的トランス作用因子が必要である。酵母では、最重要なのはUAF(upstream activating factor)、TBP(TATA-box binding protein)、CBF(core binding factor)であり、これらはプロモーターエレメントに結合して転写開始前複合体(PIC)を形成し、その後RNAポリメラーゼによって認識される。ヒトでは類似したPICがSL1(TBPとTBP随伴因子(TAF)から構成される)、転写開始因子、UBF(upstream binding factor)から組み立てられる。Pol IはrRNAの大部分(28S、18S、5.8S)の転写を担うが、5S rRNAはPol IIIによって転写される[19]。
Pol Iによる転写によって長い前駆体分子(45S pre-rRNA)が形成されるが、この分子にはまだ内部転写スペーサー領域(ITS)や外部転写スペーサー領域(ETS)が含まれており、18S、5.8S、28S RNAを作り出すためにはさらなるプロセシングが必要である。真核生物では、特定の配列と結合するガイドRNAを介した相互作用によって、RNA修飾酵素がそれぞれの認識部位へもたらされる。こうしたガイドRNAは核小体低分子RNA(snoRNA)と呼ばれるグループに属しており、タンパク質と複合体を形成してsnoRNPとして存在している。rRNAのプロセシングが行われると、リボソームサブユニットへの組み立ての準備が整った状態となるが、これらに加えてさらに5S rRNAも必要である。酵母では、5S rDNA配列はスペーサー領域に位置し、核小体内で転写される。
高等真核生物や植物では状況はより複雑であり、5S rDNA配列はNOR外に位置している。5S rRNAは核質においてPol IIIによって転写され、その後核小体でのリボソームの組み立てに加わる。この組み立てにはrRNAだけでなく、リボソームタンパク質も関与している。リボソームタンパク質をコードしている遺伝子は核質でPol IIによって転写され、一般的なタンパク質合成経路(転写、pre-mRNAプロセシング、成熟RNAの核外輸送、細胞質のリボソームによる翻訳)を経る。その後、成熟型リボソームタンパク質は核内へ、そして最終的には核小体へ輸送される。rRNAとリボソームタンパク質が結合し成熟することで、リボソームの完全な40Sサブユニット(小サブユニット)と60Sサブユニット(大サブユニット)が形成される。これらのサブユニットは核膜孔複合体を通過して細胞質へ輸送され、そこで遊離状態で存在するか、または小胞体に結合して粗面小胞体を形成する[20][21]。
ヒトの子宮内膜では、nucleolar channel system(NCS)と呼ばれる微細構造が形成されることがある。その起源や機能は明確にはなっていない[22]。
タンパク質の隔離
核小体はリボソーム生合成における役割に加えて、nucleolar detentionと呼ばれる過程によってタンパク質を捕捉して固定化することが知られている。核小体内に捕捉されたタンパク質は、拡散して結合パートナーと相互作用することができない状態となる。VHL、PML、MDM2、POLD1、RelA、HAND1、TERTなど、この翻訳後調節機構の標的となるタンパク質は多く知られている。核小体内の遺伝子間領域に由来する長鎖ノンコーディングRNAがこの現象を担っていることが明らかにされている[23]。
出典
関連文献
外部リンク
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads