銫(英語:Caesium或Cesium;舊譯鏭),是一種化學元素,其化學符號為Cs,原子序數為55,原子量為7002132905451960000♠132.90545196 u。銫是淡金色且質地極軟的鹼金屬,熔點低,28.44 ℃時即會熔化。它是在室溫或者接近室溫的條件下能呈現液態的五種金屬元素之一[註 1]。銫的物理性質和化學性質與同為鹼金屬的銣和鉀相似。該金屬極度活潑,是活性最大的金屬元素,常溫下在空氣中容易自燃,遇水會迅速發生爆炸性反應。它是具有穩定同位素的元素中電負性最低的。天然銫通常是從銫榴石中提取出來的,而其放射性同位素,尤其是銫-137,是更重元素的衰變產物,可從核反應堆產生的廢料中提取。
Quick Facts 外觀, 概況 ...
銫 55Cs|
|
| 外觀 |
|---|
金屬:淡金色
 |
| 概況 |
|---|
| 名稱·符號·序數 | 銫(Caesium)·Cs·55 |
|---|
| 元素類別 | 鹼金屬 |
|---|
| 族·週期·區 | 1·6·s |
|---|
| 標準原子質量 | 132.90545196(6)[1] |
|---|
| 電子排布 | [Xe] 6s1
2,8,18,18,8,1
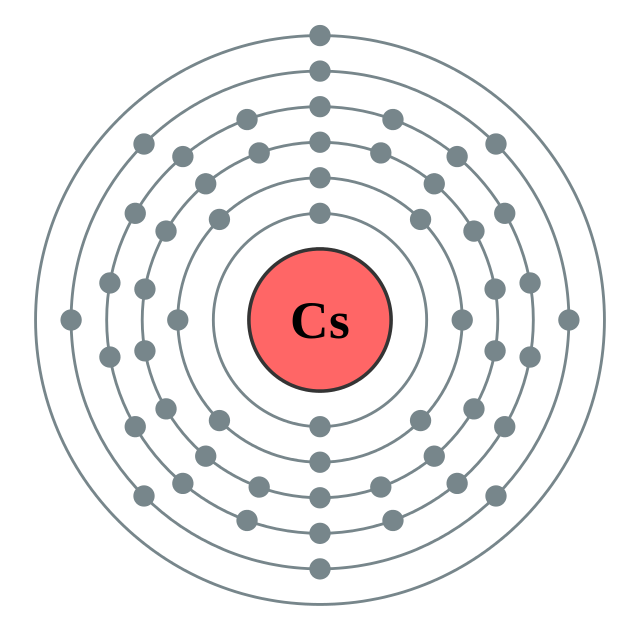 銫的電子層(2,8,18,18,8,1) 銫的電子層(2,8,18,18,8,1) |
|---|
| 歷史 |
|---|
| 發現 | 羅伯特·威廉·本生和古斯塔夫·基爾霍夫(1860年) |
|---|
| 分離 | 卡爾·賽特貝格(1882年) |
|---|
| 物理性質 |
|---|
| 物態 | 固體 |
|---|
| 密度 | (接近室溫)
1.93 g·cm−3 |
|---|
| 熔點時液體密度 | 1.843 g·cm−3 |
|---|
| 熔點 | 301.59 K,28.44 °C,83.19 °F |
|---|
| 沸點 | 944 K,671 °C,1240 °F |
|---|
| 臨界點 | 1938 K,9.4 MPa |
|---|
| 熔化熱 | 2.09 kJ·mol−1 |
|---|
| 汽化熱 | 63.9 kJ·mol−1 |
|---|
| 比熱容 | 32.210 J·mol−1·K−1 |
|---|
蒸氣壓
| 壓/Pa
|
1
|
10
|
100
|
1 k
|
10 k
|
100 k
|
| 溫/K
|
418
|
469
|
534
|
623
|
750
|
940
|
|
| 原子性質 |
|---|
| 氧化態 | -1、+1
(強鹼性) |
|---|
| 電負性 | 0.79(鮑林標度) |
|---|
| 電離能 | 第一:375.7 kJ·mol−1
第二:2234.3 kJ·mol−1
第三:3400 kJ·mol−1 |
|---|
| 原子半徑 | 265 pm |
|---|
| 共價半徑 | 244±11 pm |
|---|
| 范德華半徑 | 343 pm |
|---|
 銫的原子譜線 銫的原子譜線 |
| 雜項 |
|---|
| 晶體結構 | 體心立方 |
|---|
| 磁序 | 順磁性[2] |
|---|
| 電阻率 | (20 °C)205 n Ω·m |
|---|
| 熱導率 | 35.9 W·m−1·K−1 |
|---|
| 膨脹系數 | (25 °C)97 µm·m−1·K−1 |
|---|
| 楊氏模量 | 1.7 GPa |
|---|
| 體積模量 | 1.6 GPa |
|---|
| 莫氏硬度 | 0.2 |
|---|
| 布氏硬度 | 0.14 MPa |
|---|
| CAS號 | 7440-46-2 |
|---|
| 同位素 |
|---|
主條目:銫的同位素
|
Close
1860年,兩位德國化學家羅伯特·威廉·本生和古斯塔夫·基爾霍夫通過剛剛研究出來的焰色反應發現銫,並以拉丁文「caesius」(意為天藍色)作為新元素的名稱。銫最早的小規模應用是作為真空管以及光電池的吸氣劑。1967年,國際單位制中的秒開始以銫-133的發射光譜中一個特殊的頻率作為定義。自此之後,銫廣泛地用於原子鐘。二十世紀九十年代以來,銫元素的最大應用是用於鑽井液的甲酸銫,它在化學工業以及電子工業等領域也有重要用途。其放射性同位素銫-137的半衰期大約為30年,可以用於醫學、工業測量儀器以及水文學等。雖然銫僅有輕微的化學毒性,但銫金屬的高活潑性使之被歸類為危險性物質,而其放射性同位素則會對人體健康和環境生態造成重大危害。



